Kardiogen chock är ett utomordentligt allvarligt tillstånd med hög mortalitet även vid optimalt omhändertagande. 1-årsöverlevnaden är cirka 50 % för tidigt revaskulariserade patienter och cirka 35 % för övriga.
Detta avsnitt handlar om kardiogen chock i samband med akut myokardinfarkt. Kardiogen chock som inte presenteras som akut myokardinfarkt (akut dekompenserad kronisk hjärtsvikt, myokardit, septisk chock med sekundär myokardiell svikt, dekompenserat klaffvitium) behandlas inte här. Läs även sidan akut hjärtsvikt.
Sidoinnehåll
Bakgrund kardiogen chock
Kardiogen chock är ett tillstånd med inadekvat ändorganperfusion på grund av kardiell dysfunktion.1 Orsaken är oftast (men inte alltid) en omfattande ischemisk myokardskada i vänster kammare (STEMI eller NSTEMI), vilket medför låga slagvolymer.
Blodtryck är produkten av hjärtminutvolymen och resistansen i cirkulationen: BT = CO (hjärtminutvolym) x SVR (perifer resistans)
Kardiogen chock komplicerar idag ca 6 % av ST-höjningsinfarkter (STEMI) och ca 2,5 % av icke-ST-höjningsinfarkter (NSTEMI) och är den ledande dödsorsaken hos patienter med hjärtinfarkt som kommer levande till sjukhus.2345 Mortaliteten låg på 1970-talet på 80 %, men ligger i Sverige och andra europeiska länder idag runt 40-50 % (något högre för STEMI och något lägre för NSTEMI).64578 Egen svensk (1995-2013) och US-data (2005-2013) visar även en ökning av CS-mortalitet.910
Majoriteten av patienter som utvecklar kardiogen chock gör det efter ankomst till sjukhuset, ca 75 % inom 24 timmar.
Differentialdiagnos: chock hos patient med akut myokardinfarkt
Den typiska kardiogen-chock patienten inkommer med en akut myokardinfarkt (STEMI eller NSTEMI). Dessa patienter har, oavsett infarkttyp, en akut koronarangio-indikation. I vissa fall kommer koronarangio att visa att arbetshyptotesen myokardinfarkt var fel. Exempel på andra diagnoser i denna situationen se differentialdiagnos: Chock hos patienter utan myokardinfarkt
Var fjärde patient som utvecklar chock som komplikation till en akut myokardinfarkt har en annan kardiell chockorsak än ischemisk vänsterkammarsvikt eller, mer sällsynt, en icke-kardiogen chock orsakad av extrakardiella problem. Det är därför mycket viktig att aktivt tänka på differentialdiagnoser och rutinmässig utesluta dem vanligaste genom UCG:
Orsaker till kardiogen chock hos patienter med akut myokardinfarkt
Orsaker till kardiogen chock (=kardiella differentialdiagnoser till chock)
- Systolisk vänsterkammarsvikt (75 %)
- Mekaniska infarktkomplikationer:11
– Infarktrelaterad akut mitralisinsufficiens (chordaeruptur eller papillarmuskelruptur) (4-8 %)
– Infarktrelaterad ventrikel-septumdefekt (VSD) (5 %)
– Kammarruptur med tamponad (2 %) - Akut högerkammarinfarkt med chock (3 %)
- PCI-komplikation (dissektion (ischemi), perforation (tamponad); om chock så utvecklas det under/efter PCI)
- Sedan tidigare befintligt klaffel
- Bradykardi
- Förmaks-/kammar -takykardier
Extrakardiella orsaker till chock hos patienter med akut myokardinfarkt
Även patienter med bekräftad infarkt kan gå i chock på grund av en extrakardiell orsak. Det är viktigt att aktivt tänka på dessa extrakardiella differentialdiagnoser, till exempel hos patienter som går i chock efter PCI:
- Blödning (tex diffus på grund av antikoagulation/trombolys eller retroperitonealt efter a. femoralis-stick för PCI)
- Anafylaxi (tex röntgenkontrast i samband med angiografi)
- Läkemedel (tex betablockerare)
- Hypovolemi (tex polyuri sekundär till överdosering av diuretika)
- Pneumotorax (tex orsakad av CVK-inläggning)
Differentialdiagnos: chock hos patient utan myokardinfarkt
I vissa fall kommer koronarangiografi att visa att arbetshyptotesen myokardinfarkt var fel. Exempel på andra diagnoser i denna situationen:
- Takotsubokardiomyopati
- Akut dekompenserad kronisk hjärtsvikt
- Aortadissektion
- Lungemboli
- Perimyokardit
- Hypovolemisk chock:
- Blödning (tex diffus p g a antikoagulation eller trombolys, retroperitonealt efter a. femoralis-stick för PCI)
- Gastrointestinal förlust (diarré, kräkning)
- Renal förlust (extrem diuretika överdosering, hypoaldosteronism)
- Anafylaxi (tex röntgenkontrast i samband med angiografi)
- Läkemedel (tex betablockerare)
- Hypovolemi (tex polyuri)
- Pneumotorax (tex orsakad av CVK-inläggning)
- Septisk chock
- Metabol (acidos, hypotermi)
Diagnos
Diagnosen kardiogen chock är ofta den första arbetshypotesen för patienter med STEMI som hamnar i chock, men tänk alltid på ovan nämnda differentialdiagnoser. Hos patienter med NSTEMI är diagnosen i den kliniska vardagen ibland mindre uppenbar, samtidigt som hemodynamiskt instabila NSTEMI-patienter har en lika brådskande indikation för koronarangiografi som STEMI-patienter.
Kliniska och EKG-mässiga tecken på akut hjärtinfarkt:
- Bröstsmärta, akut dyspné eller andra symtom tydande på akut hjärtinfarkt.
- EKG-tecken på akut myokardinfarkt.
- Förhöjda hjärtskademarkörer (ofta inte möjligt att invänta svar).
- Akut UCG: regional väggrörelsestörning.
Definition av kardiogen chock
- Blodtryck < 90 mmHg under > 30 minuter (eller kortare om behandling med till exempel inotropa droger inleds).
Se stycket om normotensiv chock nedan - Låg hjärtminutvolym som inte förklaras av hypovolemi eller arytmi. (Om PA-kateter finns: cardiac index < 1,8 L/min per m2 utan stöd eller < 2,2L med stöd) och oftast höga fyllnadstryck (PCWP > 15 mmHg)2
- Tecken på vävnadshypoperfusion (oliguri < 30 ml/timme, perifer kyla, högt laktat (>2mmol/l)3, medvetandepåverkan).1
I kliniska vardagen ställs diagnosen CS på patienter med kliniska tecken på hypoperfusion (kalla extremiteter, oliguri, medvetandepåverkan, högt laktat) och en kardiell orsak, ihållande i >30 minuter utan förbättring efter volymbehandling (dvs försök att ge vätska i.v om pat inte är i lungödem) och i regelfall hypotension <90 mmHg. Notera dock att blodtryck <90 mmHg inte anses vara ett obligatoriskt kriterie: Fall med normotensiv chock där vasokonstriktion upprätthåller blodtrycket samtidigt med hypoperfusion/hypooxygenation förekommer.312
För mer detaljerat definition se: Standardized Definitions for Cardiogenic Shock Research and Mechanical Circulatory Support Devices: Scientific Expert Panel From the Shock Academic Research Consortium (SHARC) (Circulation 2023)1
Kardiogen chock motsvarar klass IV i Killip-klassifikationen av akut hjärtsvikt hos patienter med akut hjärtinfarkt.
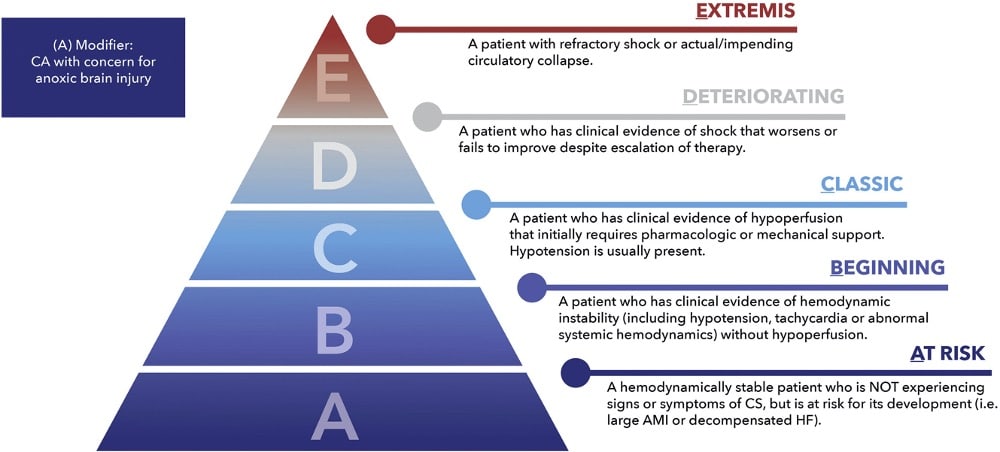
Stadier i kardiogen chock
Det US-amerikanska PCI-förbundet SCAI har 2019 utvecklat och 2022 updaterad en klassifkation som skiljer olika stadier i kardiogen chock.13. Flera studier visar att klassifikationen korrelerar med prognosen, men SCAI-klassifikationen används vanligtvis inte för beslutsfattning.14
Behandling och monitorering
Handläggning
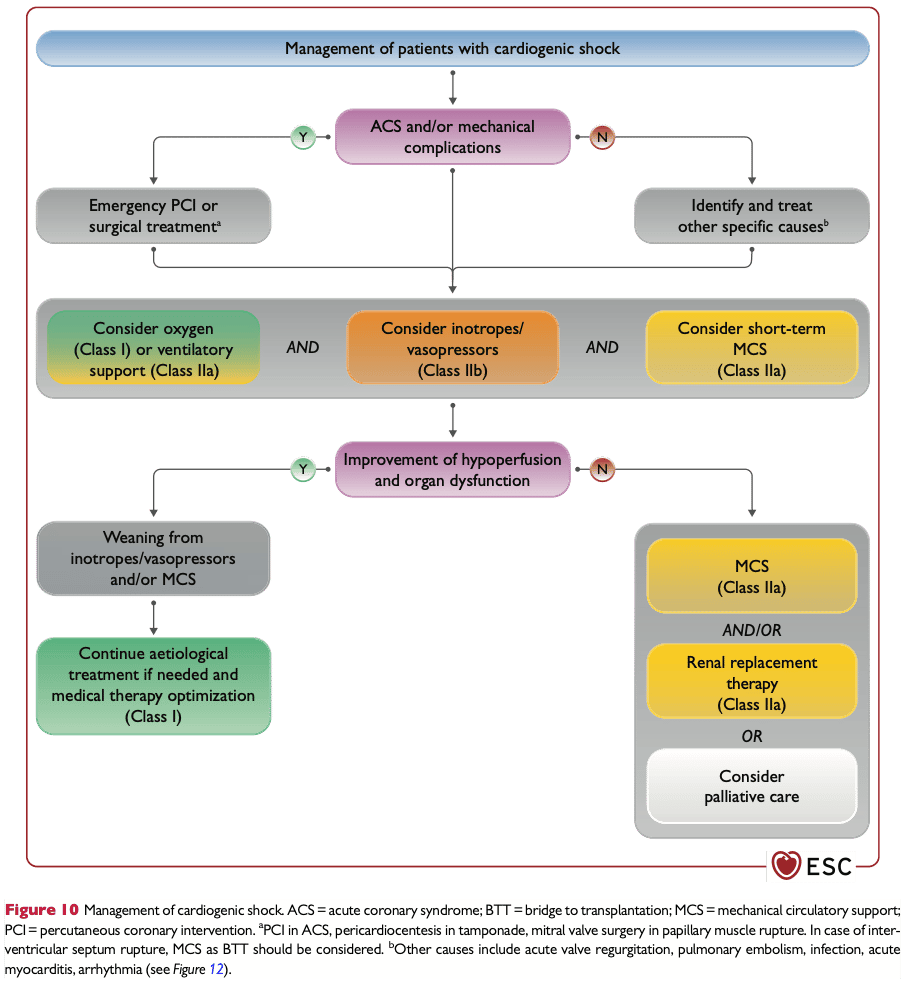
Tänk på följande vid handläggning av patienter i chock där arbetshypotesen är akut myokardinfarkt:
- Snabb transport till ett PCI-lab
Patienter med kardiogen chock i samband med båda STEMI och NSTE-ACS bör angiograferas inom 2 timmar (ESC IC).15 Prognosen är direkt beroende av tiden till PCI varför patienten snarast bör transporteras till närmaste PCI-lab. Om PCI-labbet finns på samma sjukhus rekommenderas att eventuellt nödvändiga stödjande åtgärder (tex CVK, intubation, katekolaminer, urinkateter) görs på PCI-lab, istället för att först flytta patienten till IVA eller att stanna på akuten.
Vid transport till ett annat sjukhus är målet att minska fördröjning på grund av ovan nämnda stödjande åtgärder så mycket det går.
Om patienten inte anses transportabel bör man noga beakta exakt vad det är som gör att patienten inte kan transporteras och om möjligt undanröja denna faktor. Diskussion med PCI-jour rekommenderas. I undantagsfall kan trombolys diskuteras, som dock per se är mindre effektiv än PCI vid kardiogen chock. Beroende på den lokala sjukvårdsstrukturen kan för utvalda yngre icke-transportabla patienter transport till PCI-lab med hjälp av ett inhämtat ECMO-team diskuteras, den frågan bör i så fall diskuteras i tidigt skede.
Det är av vikt att patientens underliggande riskprofil värderas innan patienten transporteras (tex ålder och komorbiditet) då detta påverkar prognosen och därför har betydelse för valet av behandlingsintensitet. - Utredning av chockorsaken
Tänk igenom differentialdiagonser. Auskultera hjärtat (bästa metod för att upptäcka en VSD). Akut översiktlig UCG bör göras på alla patienter med misstänkt kardiogen chock, som allra senast vid ankomst till PCI-lab. (ESC IC)
Läs även om differentialdiagnoser på sidan akut hjärtsvikt. - Stödjande behandling (se nedan)
Revaskularisering vid kardiogen chock
De flesta patienterna med kardiogen chock och hjärtinfarkt har en allvarlig kranskärlssjukdom, till exempel proximal LAD-stenos/ocklusion, vänster huvudstamsstenos/ocklusion eller 3-kärlssjukdom.
I SHOCK studien visade man att patienterna som erhöll revaskularisering inom 2 timmar hade bäst prognos.16 En koronarangiografi med följande revaskularisering genom PCI (alternativt akut CABG om PCI är olämpligt)17181920 är den enda kausala behandlingen.
70-80 % av patienter med infarktorsakad kardiogen chock har en koronar flerkärlssjukdom (multivessel disease).21 22 En studie från 2017 (CULPRIT-SHOCK) 23 har visat att patienter i kardiogen chock med flerkärlssjukdom har mindre risk att dö eller få terminal njursvikt om man vid initiala PCIn endast behandlar culprit lesionen och avstår från ad hoc PCI mot andra kärl (men planerar åtgärd åt andra lesioner senare i förloppet efter stabilisering). ((se section 10 in: Byrne RA et al; ESC Scientific Document Group. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-3826. doi: 10.1093/eurheartj/ehad191. PMID: 37622654.))
Monitorering
Minimum
Se till att transporten till PCI-lab inte fördröjs av dessa åtgärder. För transport till PCI-lab räcker oftast en kopplad defibrillator, POX-mätning och en blodtrycksmanschett. Resten kan sedan göras på plats.
- Artärnål för invasiv tryckmätning och provtagning (ESC IC).
- KAD för timdiures
- Akut ekokardiografisk undersökning (mekaniska komplikationer till hjärtinfarkt måste uteslutas tidigt i förloppet!)
- Ischemi- och arytmiövervak
- Mätning av SpO2
Önskvärt
- CVK för CVP-mätning och monitorering av centralvenös syrgasmättnad (SvO2)
- Pulmonaliskateter (PA-kateter) kan övervägas i vissa svårare fall om kunskap finns, för att mäta fyllnadstryck och cardiac index
Stödjande behandling
Medicinsk behandling syftande till att stabilisera patientens tillstånd är oftast otillräcklig i sig, men ändå viktig då den bidrar till att hålla patienten vid liv fram till att angiografi och eventuell intervention kan genomföras.
Syftet med behandlingen är att öka hjärtminutvolym och perifer genomblödning samt syresättning.
- Vätska
Gör alltid ett försök med i.v. vätska (>200 ml under 15-30 min) hos patienter som inte är tydligt övervätskade (rekommendation ESC IC). Patienter i chock med möjlig högerkammarinfarkt (inferiora ST-höjningar, ST-höjningar i högerkammaravledningar) kräver ofta stora mängder vätska, ge 500-1000 ml under dem första 30-60 minuterna. - Inotropa/vasoaktiva droger
Behövs oftast som en del i behandlingen. Behandling med dessa droger ska alltid ses som en kortsiktig lösning och avvecklas så snart omständigheterna tillåter.
Inget inotropt/vasoaktivt läkemedel har visat sig ha någon positiv prognostisk betydelse. Tidigare har dopamin använts/rekommenderats som förstahandspreparat vid inotrop terapi med tillägg av noradrenalin vid behov, dock visade en studie som jämförde dopamin med noradrenalin hos patienter med chock att det fanns en trend mot högre korttidsmortalitet och mer arytmier i gruppen som erhöll dopamin varför noradrenalin numera är förstahandsval.24
Förslagsvis ges noradrenalin med dosen 0,03-0,6 μg/kg/min beroende på terapeutiskt svar. Tänk dock på att eventuell blodtryckstegring oftast sker till priset av ökad syrgaskonsumtion i hjärtat. Den ökande perifera resistansen kan medföra att hjärtminutvolymen faller trots att blodtrycket stiger och kan då förvärra vävnadsacidosen. Hos patienter med bradyarytmier i kombination med kardiogen chock kan dopamin vara ett bra alternativ tills pacemakerbehandling är möjlig.
ESC guidline hjärtsvikt 2021: En vasopressor, i första hand noradrenalin, “may be considered” (ESC IIbB) vid kardiogen chock, för att öka blodtrycket och organperfusionen. I kliniska verkligheten finns det ofta inte något alternativ och noradrenalin är förstahandsbehandling vid kardiogen chock.25262728
- Trombocythämmare
Trombyl (ASA) och ADP-hämmare skall ges enligt samma rutin som vid hjärtinfarkt. Vid hjärtinfarkt som kompliceras med kardiogen chock finns dock inga studier vad gäller nyttan med trombocythämning, men de flesta författare rekommenderar en laddningsdos ASA given p.o. alternativt via ventrikelsond hos patienter med medvetandepåverkan. Den enterala resorptionen är ofta nedsatt vid CS, huruvida en generell i.v. administration av trombocythämmare (i.v. ASA, i.v. Cangrelor) ger en fördel utvärderas i en RCT. - Diuretika
Om diuresen faller eller upphör och patienten inte har någon tidigare njurinsufficiens är detta ett symtom på att njurperfusionen är otillräcklig.
Det finns inget egenvärde med att upprätthålla en viss timdiures så länge patienten inte är övervätskad. Njurfunktionen påverkas inte av nivån på diuresen. Okritiskt användande av diuretika undanröjer dessutom möjligheten att genom en enkel fysiologisk variabel, diuresen, få ett kvitto på vävnadsperfusionen.
Dopamin i så kallad diuretisk dos har ingen plats i modern intensivvård och kan hos denna patientgrupp bidra till arytmiproblem. Om patienten är övervätskad ges enklast loopdiuretikum (Furix) för att öka diuresen.
En del (ca 10-20 %) patienter med kardiogen chock har behov av vätska i.v. på grund av otillräcklig fyllnad av vänster kammare (lågt preload). Dessa patienter går att identifiera med hjälp av UCG (tom och sammanfallen vänsterkammare, sammanfallen vena cava inferior) eller PA kateter (relativt lågt PCWP, fyllnadstryck). - Respiration
2/3 av patienter i kardiogen chock orsakat av en vänsterkammarinfarkt utvecklar lungödem. CPAP-behandling kan då vara ett alternativ, men tänk på att en patient i kardiogen chock ofta är beroende av preload och att den venösa återfyllnaden till hjärtat påverkas av CPAP.
Utvärdera effekten med hjälp av kliniskt svar på behandling, SpO2 och blodgaser. I många fall kan respiratorbehandling behövas, intubering av patienter i kardiogen chock kräver då god anestesiologisk kunskap på grund av risken för allvarlig hypotension i samband med premedicinering (plus att patienten oftast inte är fastande).
Mekanisk Cirkulatorisk Support
- IABP
Intra aortic balloon pump (IABP) var under många år standardterapi vid kardiogen chock. Ballongen är (oftast på PCI-lab) inlagd via a. femoralis och ligger i aorta decendens. Ballongen är uppblåst i diastole men töms i systole. Uppblåst ballong i diastole leder till ökat blodflöde till kranskärlen och den systoliska tömningsfasen leder till en viss avlastning för hjärtat (sänker afterload). Nettoeffekten blir att slagvolym (och således hjärtminutvolym) ökar. I en studie från 2012 har användingen av IABP vid kardiogen chock utlöst av hjärtinfarkt inte kunnat förbättra överlevnad vid 30 dagar29 eller vid 6-års follow-up.30 Aktuella riktliner rekomenderar därför inte längre rutinmässig inläggning av IABP för dessa patienter (ESC-rekomendation IIIB) varför användning i Sverige har minskat kraftigt. IAPB används dock fortfarande på många centra för patienter med mekaniska infarktkomplikationer (VSD; akut mitralinsufficiens, ESC IIbC indikation vid kardiogen chock + mekanisk komplikation31.) eller som tillägg till ECMO (för att få pulsatilt flöde).
- ECMO
Extrakorporal membranoxygenering (ECMO) är en hjärtlungmaskin som sedan några år finns i bärbar storlek, det vill säga; en patient med ECMO kan transporteras från och till PCI-labbet och i vanlig ambulans eller helikopter. En venös och en arteriell infart kan oftast läggas perkutant via vena/arteria femoralis. En ECMO kräver i princip ingen hjärtfunktion, det vill säga fungerar även vid asystoli. Det finns i nuläget inga större studier som har testat ECMO-terapi varför indikationen i nuläget bara definieras enligt lokala erfarenheter.
ECMO kan vara en livsräddande behandling för få utvalda patienter varför tidig diskussion med närmaste ECMO-centrum rekommenderas för utvalda patienter vid terapiresistent progredient chock.
I 2023 visade ESCL-Shock-studien, som randomiserade 420 patienter med infarktorsakad kardiogen chock, att ECMO inte förbättrar 30-dagars mortalitet, men ökar risken för blödningskomplikationer.32
- Andra hjärtpumpar: Andra typer av mekanik assistans (Impella, Tandem Heart) finns inte rutinmässigt tillgängliga i Sverige.
Behandling av andra orsaker till kardiogen chock
Akut högerkammarinfarkt
Vid ocklusion av proximala delar av höger kranskärl kan akut högerkammarinfarkt med chock inträffa. Kliniskt är patienten hypoton och har oftast högt CVT (halsvenstas), men sällan lungödem.
EKG visar i typfallet ST-höjning i avledning V4R (högersidig bröstavledning). Diagnosen kan bekräftas med ekokardiografi. Korttidsprognosen är dålig, medan långtidsprognosen för dem som överlever den akuta sjukdomsfasen är god.
Behandlingen är baserad på följande principer, som erfarenhetsmässigt visat sig relativt framgångsrika, men som saknar stöd av randomiserade studier:
- Höger kammare är preloadberoende och volymstillförsel med målsättning
CVT ≥ 15 mmHg har varit standardrekommendation.
Patienter med högerkammarinfarkt behöver volymtillförsel, men man bör beakta att distension av höger hjärthalva påverkar vänsterkammarfunktionen negativt via septum och perikardiet. Volymexpansion kan även öka läckage i trikuspidalisklaffen. För kraftig volymexpansion kan alltså inverka negativt på hjärtminutvolymen. - Vissa författare förordar inotropi som förstahandsterapi och endast försiktig volymtillförsel. Ofta används kombinationsterapi.
- Akut angiografi och revaskularisering och eventuellt IABP.
Akut mitralinsufficiens och VSD efter hjärtinfarkt
Den akuta infarkten kompliceras ibland av mekaniska komplikationer i form av VSD eller akut mitralinsufficiens på grund av chordaeruptur.
Kliniskt ses oftast en plötslig hemodynamisk försämring och man hör tillkomst av typiskt blåsljud, ofta sker detta några dagar efter infarktsymtom-debut.
Diagnosen bekräftas med akut ekokardiografi men kan ofta ställas med stetoskopet.
Den akuta mortaliteten är utomordentligt hög, ca 1 % per timme under dem första 24 timmarna för VSD och ännu sämre för akut mitralinsufficiens som beror på chordaeruptur.
Tidig kirurgi kan rädda dessa patienter. Detta är bäst belagt för patienter med VSD orsakad av infarkt. Att vänta på att situationen stabiliseras kan vara en felaktig strategi för denna patientgrupp på grund av den mycket höga tidiga mortaliteten.33
Alla patienter med infarkt-VSD går inte omedelbart i chock. Att patienten inledningsvis mår bra är ett argument för och inte emot kirurgi.
Kliniska studier om kardiogen chock
Det finns ett mycket begränsat antal randomiserade studier i kardiogen-chock fältet. Är du intresserad av detaljer rekommenderas en lättläst översikt över alla studier fig 1 i Thiele 20213 eller fig 2 i Thiele 201934
Litteratur
SCAI/EAPCI/ACVC Expert Consensus Statement on Cardiogenic Shock in Women (2025)35
Management of cardiogenic shock. Eurointervention 202136
2023 ESC Guidelines for the management of acute coronary syndromes ((Byrne RA et al; ESC Scientific Document Group. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-3826. doi: 10.1093/eurheartj/ehad191. PMID: 37622654.))
2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure37
Treatments targeting inotropy (EHJ 2019)38
ESC guideline hjärtsvikt 201615
Epidemiology, pathophysiology and contemporary management of cardiogenicshock – a position statement from the HeartFailure Association of the European Societyof Cardiology (Eur J Heart Fail 2020)39
Management of cardiogenic shock complicating myocardial infarction: an update 201940
SCAI clinical expert consensus statement on the classification of cardiogenic shock 2019 41
PCI Strategies in Patients with Acute Myocardial Infarction and Cardiogenic Shock(CULPRIT-SHOCK) 201723
Contemporary Management of Cardiogenic Shock: A Scientific Statement From the American Heart Association 201742
Acute heart failure and cardiogenic shock: a multidisciplinary practical guidance (2016)43
Extracorporeal Life Support in Infarct-Related Cardiogenic Shock (NEJM 2023)32
Standardized Definitions for Cardiogenic Shock Research and Mechanical Circulatory Support Devices: Scientific Expert Panel From the Shock Academic Research Consortium (SHARC) (Circulation 2023)44
Se även
Last Updated on May 26, 2025 by Christian Dworeck
- ICD-söktjänst: - August 23, 2025
- Ny sida: Var blir jag citerad? - August 13, 2025
- Ny sida: PCI vid förkalkade kranskärl – teknik, tips och evidens - May 6, 2025
- Waksman R, Pahuja M, van Diepen S, Proudfoot AG, Morrow D, Spitzer E, Nichol G, Weisfeldt ML, Moscucci M, Lawler PR, Mebazaa A, Fan E, Dickert NW, Samsky M, Kormos R, Piña IL, Zuckerman B, Farb A, Sapirstein JS, Simonton C, West NEJ, Damluji AA, Gilchrist IC, Zeymer U, Thiele H, Cutlip DE, Krucoff M, Abraham WT. Standardized Definitions for Cardiogenic Shock Research and Mechanical Circulatory Support Devices: Scientific Expert Panel From the Shock Academic Research Consortium (SHARC). Circulation. 2023 Oct 3;148(14):1113-1126. doi: 10.1161/CIRCULATIONAHA.123.064527. Epub 2023 Oct 2. PMID: 37782695. [↩] [↩] [↩]
- Reynolds HR, Hochman JS. Cardiogenic shock: current concepts and improving outcomes. Circulation. 2008;117(5):686-697. doi:10.1161/CIRCULATIONAHA.106.613596 [↩] [↩]
- Thiele H, de Waha-Thiele S, Freund A, Zeymer U, Desch S, Fitzgerald S. Management of cardiogenic shock. EuroIntervention. 2021 Aug 27;17(6):451-465. doi: 10.4244/EIJ-D-20-01296. PMID: 34413010. [↩] [↩] [↩] [↩]
- Lauridsen MD, Rørth R, Lindholm MG, Kjaergaard J, Schmidt M, Møller JE, Hassager C, Torp-Pedersen C, Gislason G, Køber L, Fosbøl EL. Trends in first-time hospitalization, management, and short-term mortality in acute myocardial infarction-related cardiogenic shock from 2005 to 2017: A nationwide cohort study. Am Heart J. 2020 Nov;229:127-137. doi: 10.1016/j.ahj.2020.08.012. Epub 2020 Aug 28. PMID: 32861678. [↩] [↩]
- García-García C, Oliveras T, El Ouaddi N, Rueda F, Serra J, Labata C, Ferrer M, Cediel G, Montero S, Martínez MJ, Resta H, de Diego O, Vila J, Dégano IR, Elosua R, Lupón J, Bayes-Genis A. Short- and Long-Term Mortality Trends in STEMI-Cardiogenic Shock over Three Decades (1989-2018): The Ruti-STEMI-Shock Registry. J Clin Med. 2020 Jul 27;9(8):2398. doi: 10.3390/jcm9082398. PMID: 32727034; PMCID: PMC7465647. [↩] [↩]
- Redfors B, Angerås O, Råmunddal T, et al. 17-year trends in incidence and prognosis of cardiogenic shock in patients with acute myocardial infarction in western Sweden. Int J Cardiol. 2015;185:256-262. doi:10.1016/j.ijcard.2015.03.106 [↩]
- Thiele H, Zeymer U, Neumann FJ, Ferenc M, Olbrich HG, Hausleiter J, Richardt G, Hennersdorf M, Empen K, Fuernau G, Desch S, Eitel I, Hambrecht R, Fuhrmann J, Böhm M, Ebelt H, Schneider S, Schuler G, Werdan K; IABP-SHOCK II Trial Investigators. Intraaortic balloon support for myocardial infarction with cardiogenic shock. N Engl J Med. 2012 Oct 4;367(14):1287-96. doi: 10.1056/NEJMoa1208410. Epub 2012 Aug 26. PMID: 22920912. [↩]
- Thiele H, Akin I, Sandri M, Fuernau G, de Waha S, Meyer-Saraei R, Nordbeck P, Geisler T, Landmesser U, Skurk C, Fach A, Lapp H, Piek JJ, Noc M, Goslar T, Felix SB, Maier LS, Stepinska J, Oldroyd K, Serpytis P, Montalescot G, Barthelemy O, Huber K, Windecker S, Savonitto S, Torremante P, Vrints C, Schneider S, Desch S, Zeymer U; CULPRIT-SHOCK Investigators. PCI Strategies in Patients with Acute Myocardial Infarction and Cardiogenic Shock. N Engl J Med. 2017 Dec 21;377(25):2419-2432. doi: 10.1056/NEJMoa1710261. Epub 2017 Oct 30. PMID: 29083953. [↩]
- Redfors B, Angerås O, Råmunddal T, Dworeck C, Haraldsson I, Ioanes D, Petursson P, Libungan B, Odenstedt J, Stewart J, Lodin E, Wahlin M, Albertsson P, Matejka G, Omerovic E. 17-year trends in incidence and prognosis of cardiogenic shock in patients with acute myocardial infarction in western Sweden. Int J Cardiol. 2015 Apr 15;185:256-62. doi: 10.1016/j.ijcard.2015.03.106. Epub 2015 Mar 10. PMID: 25814213. [↩]
- Wayangankar SA, Bangalore S, McCoy LA, Jneid H, Latif F, Karrowni W, Charitakis K, Feldman DN, Dakik HA, Mauri L, Peterson ED, Messenger J, Roe M, Mukherjee D, Klein A. Temporal Trends and Outcomes of Patients Undergoing Percutaneous Coronary Interventions for Cardiogenic Shock in the Setting of Acute Myocardial Infarction: A Report From the CathPCI Registry. JACC Cardiovasc Interv. 2016 Feb 22;9(4):341-351. doi: 10.1016/j.jcin.2015.10.039. Epub 2016 Jan 20. PMID: 26803418. [↩]
- Hochman JS, Buller CE, Sleeper LA, Boland J, Dzavik V, Sanborn TA, Godfrey E, White HD, Lim J, LeJemtel T. Cardiogenic shock complicating acute myocardial infarction–etiologies, management and outcome: a report from the SHOCK Trial Registry. SHould we emergently revascularize Occluded Coronaries for cardiogenic shocK? J Am Coll Cardiol. 2000 Sep;36(3 Suppl A):1063-70. doi: 10.1016/s0735-1097(00)00879-2. PMID: 10985706. [↩]
- Chioncel O, Parissis J, Mebazaa A, Thiele H, Desch S, Bauersachs J, Harjola VP, Antohi EL, Arrigo M, Gal TB, Celutkiene J, Collins SP, DeBacker D, Iliescu VA, Jankowska E, Jaarsma T, Keramida K, Lainscak M, Lund LH, Lyon AR, Masip J, Metra M, Miro O, Mortara A, Mueller C, Mullens W, Nikolaou M, Piepoli M, Price S, Rosano G, Vieillard-Baron A, Weinstein JM, Anker SD, Filippatos G, Ruschitzka F, Coats AJS, Seferovic P. Epidemiology, pathophysiology and contemporary management of cardiogenic shock – a position statement from the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail. 2020 Aug;22(8):1315-1341. doi: 10.1002/ejhf.1922. Epub 2020 Jul 16. Erratum in: Eur J Heart Fail. 2021 Feb;23(2):345. PMID: 32469155. [↩]
- Baran DA, Grines CL, Bailey S, Burkhoff D, Hall SA, Henry TD, Hollenberg SM, Kapur NK, O’Neill W, Ornato JP, Stelling K, Thiele H, van Diepen S, Naidu SS. SCAI clinical expert consensus statement on the classification of cardiogenic shock: This document was endorsed by the American College of Cardiology (ACC), the American Heart Association (AHA), the Society of Critical Care Medicine (SCCM), and the Society of Thoracic Surgeons (STS) in April 2019. Catheter Cardiovasc Interv. 2019 Jul 1;94(1):29-37. doi: 10.1002/ccd.28329. Epub 2019 May 19. PMID: 31104355. [↩] [↩]
- se översikt över studier i tabell 2 in: Thiele H, de Waha-Thiele S, Freund A, Zeymer U, Desch S, Fitzgerald S. Management of cardiogenic shock. EuroIntervention. 2021 Aug 27;17(6):451-465. doi: 10.4244/EIJ-D-20-01296. PMID: 34413010. [↩]
- Ponikowski P, Voors AA, Anker SD, Bueno H, Cleland JGF, Coats AJS, Falk V, González-Juanatey JR, Harjola VP, Jankowska EA, Jessup M, Linde C, Nihoyannopoulos P, Parissis JT, Pieske B, Riley JP, Rosano GMC, Ruilope LM, Ruschitzka F, Rutten FH, van der Meer P; ESC Scientific Document Group. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC)Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J. 2016 Jul 14;37(27):2129-2200. doi: 10.1093/eurheartj/ehw128. Epub 2016 May 20. Erratum in: Eur Heart J. 2016 Dec 30;: PMID: 27206819. [↩] [↩]
- Hochman JS, Sleeper LA, Webb JG, et al. Early revascularization in acute myocardial infarction complicated by cardiogenic shock. SHOCK Investigators. Should We Emergently Revascularize Occluded Coronaries for Cardiogenic Shock. N Engl J Med. 1999;341(9):625-634. doi:10.1056/NEJM199908263410901 [↩]
- Mehta RH, Lopes RD, Ballotta A, Frigiola A, Sketch MH Jr, Bossone E, Bates ER. Percutaneous coronary intervention or coronary artery bypass surgery for cardiogenic shock and multivessel coronary artery disease? Am Heart J. 2010 Jan;159(1):141-7. doi: 10.1016/j.ahj.2009.10.035. PMID: 20102880. [↩]
- Sousa-Uva M, Neumann FJ, Ahlsson A, Alfonso F, Banning AP, Benedetto U, Byrne RA, Collet JP, Falk V, Head SJ, Jüni P, Kastrati A, Koller A, Kristensen SD, Niebauer J, Richter DJ, Seferovic PM, Sibbing D, Stefanini GG, Windecker S, Yadav R, Zembala MO; ESC Scientific Document Group. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur J Cardiothorac Surg. 2019 Jan 1;55(1):4-90. doi: 10.1093/ejcts/ezy289. PMID: 30165632. [↩]
- Ibanez B, James S, Agewall S, Antunes MJ, Bucciarelli-Ducci C, Bueno H, Caforio ALP, Crea F, Goudevenos JA, Halvorsen S, Hindricks G, Kastrati A, Lenzen MJ, Prescott E, Roffi M, Valgimigli M, Varenhorst C, Vranckx P, Widimský P; ESC Scientific Document Group. 2017 ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation: The Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J. 2018 Jan 7;39(2):119-177. doi: 10.1093/eurheartj/ehx393. PMID: 28886621. [↩]
- Collet JP, Thiele H, Barbato E, Barthélémy O, Bauersachs J, Bhatt DL, Dendale P, Dorobantu M, Edvardsen T, Folliguet T, Gale CP, Gilard M, Jobs A, Jüni P, Lambrinou E, Lewis BS, Mehilli J, Meliga E, Merkely B, Mueller C, Roffi M, Rutten FH, Sibbing D, Siontis GCM; ESC Scientific Document Group. 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur Heart J. 2021 Apr 7;42(14):1289-1367. doi: 10.1093/eurheartj/ehaa575. Erratum in: Eur Heart J. 2021 May 14;42(19):1908. Erratum in: Eur Heart J. 2021 May 14;42(19):1925. Erratum in: Eur Heart J. 2021 May 13;: PMID: 32860058. [↩]
- Thiele H, de Waha-Thiele S, Freund A, Zeymer U, Desch S, Fitzgerald S. Management of cardiogenic shock. EuroIntervention. 2021 Aug 27;17(6):451-465. doi: 10.4244/EIJ-D-20-01296. PMID: 34413010. [↩]
- se section 10 in: Byrne RA et al; ESC Scientific Document Group. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-3826. doi: 10.1093/eurheartj/ehad191. PMID: 37622654. [↩]
- Thiele H, Akin I, Sandri M, et al. PCI Strategies in Patients with Acute Myocardial Infarction and Cardiogenic Shock. N Engl J Med. 2017;377(25):2419-2432. doi:10.1056/NEJMoa1710261 [↩] [↩]
- De Backer D, Biston P, Devriendt J, et al. Comparison of dopamine and norepinephrine in the treatment of shock. N Engl J Med. 2010;362(9):779-789. doi:10.1056/NEJMoa0907118 [↩]
- Avsnitt 11.3.6 in: McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, Burri H, Butler J, Čelutkienė J, Chioncel O, Cleland JGF, Coats AJS, Crespo-Leiro MG, Farmakis D, Gilard M, Heymans S, Hoes AW, Jaarsma T, Jankowska EA, Lainscak M, Lam CSP, Lyon AR, McMurray JJV, Mebazaa A, Mindham R, Muneretto C, Francesco Piepoli M, Price S, Rosano GMC, Ruschitzka F, Kathrine Skibelund A; ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021 Aug 27:ehab368. doi: 10.1093/eurheartj/ehab368. Epub ahead of print. PMID: 34447992. [↩]
- De Backer D, Biston P, Devriendt J, Madl C, Chochrad D, Aldecoa C, Brasseur A, Defrance P, Gottignies P, Vincent JL; SOAP II Investigators. Comparison of dopamine and norepinephrine in the treatment of shock. N Engl J Med. 2010 Mar 4;362(9):779-89. doi: 10.1056/NEJMoa0907118. PMID: 20200382. [↩]
- Levy B, Clere-Jehl R, Legras A, Morichau-Beauchant T, Leone M, Frederique G, Quenot JP, Kimmoun A, Cariou A, Lassus J, Harjola VP, Meziani F, Louis G, Rossignol P, Duarte K, Girerd N, Mebazaa A, Vignon P; Collaborators. Epinephrine Versus Norepinephrine for Cardiogenic Shock After Acute Myocardial Infarction. J Am Coll Cardiol. 2018 Jul 10;72(2):173-182. doi: 10.1016/j.jacc.2018.04.051. PMID: 29976291. [↩]
- Léopold V, Gayat E, Pirracchio R, Spinar J, Parenica J, Tarvasmäki T, Lassus J, Harjola VP, Champion S, Zannad F, Valente S, Urban P, Chua HR, Bellomo R, Popovic B, Ouweneel DM, Henriques JPS, Simonis G, Lévy B, Kimmoun A, Gaudard P, Basir MB, Markota A, Adler C, Reuter H, Mebazaa A, Chouihed T. Epinephrine and short-term survival in cardiogenic shock: an individual data meta-analysis of 2583 patients. Intensive Care Med. 2018 Jun;44(6):847-856. doi: 10.1007/s00134-018-5222-9. Epub 2018 Jun 1. Erratum in: Intensive Care Med. 2018 Nov;44(11):2022-2023. PMID: 29858926. [↩]
- Thiele H, Zeymer U, Neumann FJ, et al. Intraaortic balloon support for myocardial infarction with cardiogenic shock. N Engl J Med. 2012;367(14):1287-1296. doi:10.1056/NEJMoa1208410 [↩]
- Thiele H, Zeymer U, Thelemann N, Neumann FJ, Hausleiter J, Abdel-Wahab M, Meyer-Saraei R, Fuernau G, Eitel I, Hambrecht R, Böhm M, Werdan K, Felix SB, Hennersdorf M, Schneider S, Ouarrak T, Desch S, de Waha-Thiele S; IABPSHOCK II Trial (Intraaortic Balloon Pump in Cardiogenic Shock II) Investigators. Intraaortic Balloon Pump in Cardiogenic Shock Complicating Acute Myocardial Infarction: Long-Term 6-Year Outcome of the Randomized IABP-SHOCK II Trial. Circulation. 2018 Nov 11. doi: 10.1161/CIRCULATIONAHA.118.038201. Epub ahead of print. PMID: 30586721. [↩]
- Avsnitt 11.3.10 in: McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, Burri H, Butler J, Čelutkienė J, Chioncel O, Cleland JGF, Coats AJS, Crespo-Leiro MG, Farmakis D, Gilard M, Heymans S, Hoes AW, Jaarsma T, Jankowska EA, Lainscak M, Lam CSP, Lyon AR, McMurray JJV, Mebazaa A, Mindham R, Muneretto C, Francesco Piepoli M, Price S, Rosano GMC, Ruschitzka F, Kathrine Skibelund A; ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021 Aug 27:ehab368. doi: 10.1093/eurheartj/ehab368. Epub ahead of print. PMID: 34447992. [↩]
- Thiele H, Zeymer U, Akin I, Behnes M, Rassaf T, Mahabadi AA, Lehmann R, Eitel I, Graf T, Seidler T, Schuster A, Skurk C, Duerschmied D, Clemmensen P, Hennersdorf M, Fichtlscherer S, Voigt I, Seyfarth M, John S, Ewen S, Linke A, Tigges E, Nordbeck P, Bruch L, Jung C, Franz J, Lauten P, Goslar T, Feistritzer HJ, Pöss J, Kirchhof E, Ouarrak T, Schneider S, Desch S, Freund A; ECLS-SHOCK Investigators. Extracorporeal Life Support in Infarct-Related Cardiogenic Shock. N Engl J Med. 2023 Oct 5;389(14):1286-1297. doi: 10.1056/NEJMoa2307227. Epub 2023 Aug 26. PMID: 37634145. [↩] [↩]
- Crenshaw BS, Granger CB, Birnbaum Y, et al. Risk factors, angiographic patterns, and outcomes in patients with ventricular septal defect complicating acute myocardial infarction. GUSTO-I (Global Utilization of Streptokinase and TPA for Occluded Coronary Arteries) Trial Investigators. Circulation. 2000;101(1):27-32. doi:10.1161/01.cir.101.1.27 [↩]
- Thiele H, Ohman EM, de Waha-Thiele S, Zeymer U, Desch S. Management of cardiogenic shock complicating myocardial infarction: an update 2019. Eur Heart J. 2019 Aug 21;40(32):2671-2683. doi: 10.1093/eurheartj/ehz363. PMID: 31274157. [↩]
- Baron SJ, Chou JC, Shah T, Vest AR ¶, Abbott JD, Alasnag M †, Aurigemma C †, Barbato E †, Bellumkonda L, Bortnick AE ‡, Chieffo A †, van Geuns RJ †, Grines CL, Halvorsen S §, Hassager C §, Kapur NK, Naidu SS, Ng VG, Saw J, Lansky AJ. SCAI/EAPCI/ACVC Expert Consensus Statement on Cardiogenic Shock in Women. EuroIntervention. 2025 May 20:EIJ-D-24-01126. doi: 10.4244/EIJ-D-24-01126. Epub ahead of print. PMID: 40387531. [↩]
- Thiele H, de Waha-Thiele S, Freund A, Zeymer U, Desch S, Fitzgerald S. Management of cardiogenic shock. EuroIntervention. 2021 Aug 27;17(6):451-465. doi: 10.4244/EIJ-D-20-01296. PMID: 34413010. [↩]
- McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, Burri H, Butler J, Čelutkienė J, Chioncel O, Cleland JGF, Coats AJS, Crespo-Leiro MG, Farmakis D, Gilard M, Heymans S, Hoes AW, Jaarsma T, Jankowska EA, Lainscak M, Lam CSP, Lyon AR, McMurray JJV, Mebazaa A, Mindham R, Muneretto C, Francesco Piepoli M, Price S, Rosano GMC, Ruschitzka F, Kathrine Skibelund A; ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021 Aug 27:ehab368. doi: 10.1093/eurheartj/ehab368. Epub ahead of print. PMID: 34447992. [↩]
- Maack C, Eschenhagen T, Hamdani N, Heinzel FR, Lyon AR, Manstein DJ, Metzger J, Papp Z, Tocchetti CG, Yilmaz MB, Anker SD, Balligand JL, Bauersachs J, Brutsaert D, Carrier L, Chlopicki S, Cleland JG, de Boer RA, Dietl A, Fischmeister R, Harjola VP, Heymans S, Hilfiker-Kleiner D, Holzmeister J, de Keulenaer G, Limongelli G, Linke WA, Lund LH, Masip J, Metra M, Mueller C, Pieske B, Ponikowski P, Ristić A, Ruschitzka F, Seferović PM, Skouri H, Zimmermann WH, Mebazaa A. Treatments targeting inotropy. Eur Heart J. 2019 Nov 21;40(44):3626-3644. doi: 10.1093/eurheartj/ehy600. PMID: 30295807; PMCID: PMC7963133. [↩]
- Chioncel O, Parissis J, Mebazaa A, Thiele H, Desch S, Bauersachs J, Harjola VP, Antohi EL, Arrigo M, Gal TB, Celutkiene J, Collins SP, DeBacker D, Iliescu VA, Jankowska E, Jaarsma T, Keramida K, Lainscak M, Lund LH, Lyon AR, Masip J, Metra M, Miro O, Mortara A, Mueller C, Mullens W, Nikolaou M, Piepoli M, Price S, Rosano G, Vieillard-Baron A, Weinstein JM, Anker SD, Filippatos G, Ruschitzka F, Coats AJS, Seferovic P. Epidemiology, pathophysiology and contemporary management of cardiogenic shock – a position statement from the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail. 2020 Aug;22(8):1315-1341. doi: 10.1002/ejhf.1922. Epub 2020 Jul 16. Erratum in: Eur J Heart Fail. 2021 Feb;23(2):345. PMID: 32469155. [↩]
- Thiele H, Ohman EM, de Waha-Thiele S, Zeymer U, Desch S. Management of cardiogenic shock complicating myocardial infarction: an update 2019. Eur Heart J. 2019;40(32):2671-2683. doi:10.1093/eurheartj/ehz363 [↩]
- Baran DA, Grines CL, Bailey S, et al. SCAI clinical expert consensus statement on the classification of cardiogenic shock: This document was endorsed by the American College of Cardiology (ACC), the American Heart Association (AHA), the Society of Critical Care Medicine (SCCM), and the Society of Thoracic Surgeons (STS) in April 2019. Catheter Cardiovasc Interv. 2019;94(1):29-37. doi:10.1002/ccd.28329 [↩]
- van Diepen S, Katz JN, Albert NM, et al. Contemporary Management of Cardiogenic Shock: A Scientific Statement From the American Heart Association. Circulation. 2017;136(16):e232-e268. doi:10.1161/CIR.0000000000000525 [↩]
- Mebazaa A, Tolppanen H, Mueller C, Lassus J, DiSomma S, Baksyte G, Cecconi M, Choi DJ, Cohen Solal A, Christ M, Masip J, Arrigo M, Nouira S, Ojji D, Peacock F, Richards M, Sato N, Sliwa K, Spinar J, Thiele H, Yilmaz MB, Januzzi J. Acute heart failure and cardiogenic shock: a multidisciplinary practical guidance. Intensive Care Med. 2016 Feb;42(2):147-63. doi: 10.1007/s00134-015-4041-5. Epub 2015 Sep 14. PMID: 26370690. [↩]
- Waksman R, Pahuja M, van Diepen S, Proudfoot AG, Morrow D, Spitzer E, Nichol G, Weisfeldt ML, Moscucci M, Lawler PR, Mebazaa A, Fan E, Dickert NW, Samsky M, Kormos R, Piña IL, Zuckerman B, Farb A, Sapirstein JS, Simonton C, West NEJ, Damluji AA, Gilchrist IC, Zeymer U, Thiele H, Cutlip DE, Krucoff M, Abraham WT. Standardized Definitions for Cardiogenic Shock Research and Mechanical Circulatory Support Devices: Scientific Expert Panel From the Shock Academic Research Consortium (SHARC). Circulation. 2023 Oct 3;148(14):1113-1126. doi: 10.1161/CIRCULATIONAHA.123.064527. Epub 2023 Oct 2. PMID: 37782695. [↩]

