Sidoinnehåll
- 1 Sammanfattning hyperkolesterolemi
- 2 Bakgrund
- 3 Indikation för medikamentell lipidbehandling
- 4 Mätning av kolesterol/lipoproteiner
- 5 När behandla hyperkolesterolemi? Intervention beroende på risk och LDL-C
- 6 Målvärde för lipidbehandling
- 7 Livsstilsfaktorernas roll i kolesterolbehandling
- 8 Läkemedelsbehandling vid hyperkolesterolemi
- 9 Familjär Hyperkolesterolemi (FH)
- 10 Litteratur
Sammanfattning hyperkolesterolemi
LDL-kolesterol (LDL-C) är en kausal orsaksfaktor för utveckling av ateroskleros, minskning av LDL-C hos riskpatienter minskar kardiovaskulär mortalitet, se avsnitt bakgrund. LDL är ett av flera lipoproteiner.
Första steget i beslutsfattning angående eventuell indikation för lipidbehandling är att bedöma personens kardiovaskulära risk (ingruppering i en risk-kategori): För patienter med en sekundärpreventiv indikation kan denna bedömning göras här på sidan i avsnitt bedömning av kardiovaskulär risk. För personer där du funderar på primärpreventiv indikation ska riskvärderingsverktyget Score användas: se separata sidan om Score.
Personens risk-kategori använder du sen för att slå upp det individuella målvärdet i LDL (eller i non-HDL-C, ApoB). Sedan ser du i avsnitt “när behandla” (table 5) om det finns indikation för livsstilsinterventioner eller läkemedelsbehandling.
I sista avsnittet finns en kort sammanfattning om familjär hyperkolesterolemi.
Bakgrund
Var fjärde dödsfall i industriländer orsakas idag av aterosklerotisk kranskärlssjukdom.1 Ett århundrade av forskning2 har identifierat kolesterol-tranporterande low-density lipoprotein (LDL) som en nyckelfaktor: inlagring av LDL-kolesterol i artärväggen anses idag vara en kausal orsaksfaktor i utvecklingen av ateroskleros.3 Omfattande evidens visar att det finns ett dosberoende samband mellan LDL-kolesterol och risken för aterosklerotisk hjärt- och kärlsjukdom. Minskning av LDL-kolesterol, oavsett metod, resulterar i en proportionell minskning av ateroskleros-risken: Ju lägre LDL-kolesterol koncentration i plasma, desto lägre risk för ateroskleros-orsakade kardiovaskulära events, utan någon idag känd lägsta LDL-nivå när denna minskning av risken skulle avta.34 För varje 1 mmol/l LDL-sänkning minskade statinbehandling major vascular events5 med 22 %, död i kranskärls-sjukdom med 20 % och totalmortalitet med 10 % över 5 år. Denna relativa effekt är likadan i alla subgrupper, så att den absoluta riskreduktionen såklart är mindre hos patienter med mindre absolut risk, alltså mindre hos personer som behandlas primärpreventivt.6
Den totala aterosklerotiska plack-bördan anses vara proportionell till LDL-koncentrationen och LDL-exponeringstiden.7 Det är därför viktigt att inte bara behandla kolesterol-nivåer när ateroskleros redan har orsakat en kardiovaskulär sjukdom (sekundärprevention), men ännu viktigare att tidigt behandla, med först livsstilsinterventioner och sedan läkemedelsbehandling, personer med ökad risk för framtida aterosklerotisk kardiovaskulär sjukdom.48
ESC har 2019 (ESC 2019 Guidelines on Dyslipidaemias) aktualiserat målvärden för lipidbehandling.
Lipoproteiner
Lipoproteiner i plasma transporterar lipider: Triglycerider från tarm och lever till fettvävnad och muskulatur för förbrukning, kolesterol till levern för gallproduktion och bland annat till cellmembranen som behöver kolesterol för sin struktur och funktion.9 Alla plasma-lipoproteiner är globulära partiklar uppbyggda av ett yttre skal av ett par hundra fosfolipidmolekyler och ett stort amfibiskt (båda hydrofilt och hydrofobt, för att kunna transportera hydrofoba lipider i plasma) protein, apolipoprotein A (ApoA) eller apolipoprotein B (ApoB). På insidan transporterar denna glob kolesterol-ester molekyler.
LDL är ett av sex lipoproteiner som grupperas i olika klasser beroende på densitet:
| Densitet g/ml | Storlek nm | Innehåller Kolesterol- ester % | Innehåller Triglycerider % | Kolesterol i plasma hos en frisk person mmol/l | Protein | |
|---|---|---|---|---|---|---|
| Chylomikroner | <0,95 | 100-1000 | 2-4 | 90-95 | 0 | ApoB |
| VLDL very low-density lipoprotein | <1,006 | 40-50 | 8-14 | 50-65 | 0,1-0,4 | ApoB |
| IDL intermediate-density lipoprotein | 1,006-1,019 | 25-30 | 20-35 | 25-40 | 0,1-0,3 | ApoB |
| LDL low-density lipoprotein | 1,019-1,063 | 20-25 | 34-35 | 4-6 | 1,5-3,5 | ApoB |
| HDL high-density lipoprotein | 1,063-1,210 | 6-10 | 10-20 | 7 | 0,9-1,6 | ApoA |
| Lp(a) Lipoprotein(a) | 1,051-1,082 | 25 | 35-46 | 4-8 | ApoB |
Historien med LDL2 började 1954 när John Gofman, en läkare på Berkerley Universitetet, använde en nyligen uppfunnen ultracentrifug för att separera lipoproteiner i plasma efter lipoproteiners densitet: Han kunde identifiera två olika fraktioner, en med hög densitet (HDL) och med låg (LDL). När han sedan analyserade plasma från hjärtinfarktpatienter hittade han, jämfört med friska individer, en rejäl ökning av LDL-fraktionen (och minskning av HDL): Hyperlipoproteinemi.1112
LDL är ett cirka 20 nm stort lipoprotein, skalet uppbyggt av ett par hundra fosfolipidmolekyler och ApoB, som på insidan transporterar cirka 1500 kolesterol-ester molekyler och ansvarar för största andelen av kolesterol-transporten i blodet.2 LDL transporterar kolesterol till artärväggen, när för mycket anländer kan aterosklerosprocessen sättas igång.1314
Av alla sex lipoproteiner är alla utom HDL uppbyggda av ApoB, medan HDL innehåller ett annat protein; ApoA. Endast lipoproteiner som innehåller ApoB och som är mindre än 70 nm (alla utom chylomikroner) kan passera den endoteliala barriären. 15Även koncentrationen av ApoB (som markör för alla ApoB-innhållnade lipoproteiner) är, som LDL, associerad med ökad risk för ateroskleros: Alla Apo-B innehållande lipoproteiner (Chylomikroner, VLDL, IDL, LDL, Lp(a) ) bidrar till ateroskleros-risken, men LDL är den viktigaste eftersom att LDL transporterar den allra största andelen av kolesterolet. Eftersom varje lipoprotein innehåller endast ett protein är ApoB även en markör för det absoluta antalet LDL-partiklar i blodet.4. Varje LDL-partikel transporterar en definierad mängd kolesterolmolekyler så att antal LDL-partiklar är proportionell till mängd LDL-kolesterol i blodet, och därmed minskar LDL-partiklar konkordant med minskning av LDL-kolesterol.
Indikation för medikamentell lipidbehandling
Indikation för medikamentell lipidbehandling styrs av två faktorer: Kolesterolnivå och patientens kardiovaskulära risk:
Bedömning av den kardiovaskulära risken
Den kardiovaskulära risken ska bedömas hos alla patienter där man funderar på indikation för lipidbehandling vid hyperkolesterolemi. Detta kan ske på två sätt:
- Patienten har redan en känd hög/mycket hög kardiovaskulär risk:
- Indikation sekundärprevention för en redan diagnostiserad aterosklerotisk kardiovaskulär sjukdom:
Vilka sjukdomar menas: Se tabell 2 i nästa avsnitt “riskkategorier“, rad om “mycket hög risk” - Sjukdom som likställs med mycket hög risk att utveckla en aterosklerotisk kardiovaskulär sjukdom:
Vilka sjukdomar menas: Se tabell 2 i nästa avsnitt “riskkategorier“, rad om “mycket hög risk” och rad om “hög risk”
- Indikation sekundärprevention för en redan diagnostiserad aterosklerotisk kardiovaskulär sjukdom:
- Tills synes kardiovaskulärt friska personer (utan kriterier under 1.):
- Använd ESCs SCORE för att skatta den kardiovaskulära risken: Se sidan om SCORE här. Gå direkt till quick-calculator här.
Första frågan vid riskbedömningen är alltså om lipidbehandling gäller primär– eller sekundärprevention.
Vid primärprevention bedöms först den kardiovaskulära risken, genom att använda ESCs SCORE-vertyg (där LDL och HDL ingår): Se sidan om Score för beräkning. Undantagen är personer med LDL ≥ 4,9 mmol/l som har en indikation för statinbehandling oberoende av beräknat SCORE värde.
Vid sekundärprevention (kriterier se tabell 2) är alltid båda livsstilsintervention och medikamentell lipidbehanling indicerat. Patienter som du träffar inneliggande för ett akut koronart syndrom eller som du träffar på kardiologmottagning för en känd kranskärlssjukdom har alltså alltid en indiaktion för lipid-läkemedelsbehandling och behöver inte riskvärderas med Score.
Riskkategorier
| Riskkategori | Beräknad Score (Risk för kardio- vaskulär död inom 10 år) | Diagnoser som kvalificerar för riskkategorisering |
|---|---|---|
| Mycket hög risk | ≥10 % | 1. Dokumenterad aterosklerotisk kardiovaskulär sjukdom (“Sekundärprevention”): *Tidigare infarkt/akut koronart syndrom (som beror på ateroskleros, dvs inte t.ex. spontandissektioner) *Stabil angina *Tidigare koronar (CABG, PCI) eller annan arteriell revaskularisering *Dokumenterat relevant ateroskleros (plack) på koronarangiografi eller DT-hjärta *Ischemisk stroke , TIA (ej kardioembolisk) *Abdominellt aorta-aneurysm, perifer artärsjukdom 2. Primärprevention: Diabetes + organskada (mikroalbubinuri, retinopati, neuropati) eller + ≥ tre riskfaktorer eller om vid DM-1 över 20 år Kronisk njursvikt (eGFR <30 mL/min/1.73 m2) Familjär hyperkolesterolemi + en riskfaktor |
| Hög risk | ≥5 – 10 % | Familjär hyperkolesterolemi utan annan riskfaktor Diabetes + en annan riskfaktor eller DM-1 över 10 år Kronisk njursvikt (eGFR 30-59 mL/min/1.73 m2) Totalkolesterol > 8 mmol/l eller LDL >4,9 mmol/l Systoliskt blodtryck >180 mmHg |
| Moderat risk | ≥1 – 5 % | Diabetes: Unga patienter (T1DM <35 år; T2DM <50 år) som har haft diabetes i <10 år och som inte har andra riskfaktorer |
| Låg risk | <1 % |
ESC-tabell 2019: Riskkategorier4

Mätning av kolesterol/lipoproteiner
Ett vanligt kolesterolstatus består av fyra plasma-parametrar:
- Totalkolesterol (TC)
- LDL-C
- HDL-C
- Triglycerider (TG)
Tänk på att, vid höga LDL-C, även utesluta vanliga orsaker för sekundär hyperkolesterolemi: Hypothyreos och nefrotiskt syndrom (ta TSH, krea, urinsticka, glukos, transaminaser).16
För beräkning av ESCs Score används TC och HDL-C, LDL-C är den mest använda parametern för initiering och uppföljning av behandlingen och triglycerider används inte minst av mät-tekniska skäl (se LDL nedan):
LDL
LDL mäts för att skatta den aterosklerotiska risken som kan modifieras med LDL-C interventioner (livsstil + läkemedel). Det som ett vanligt serum-kolesterolstatus faktiskt mäter är koncentrationen av TC, HDL-C och TG, medan LDL-C beräknas av dessa mätvärden enligt Friedewald formeln17:18
LDL-C= TC – HDL-C – (TG/2.2) (allt i mmol/l)
LDL mäts alltså inte, men beräknas. Formeln kan dock underskatta LDL-värdet vid TG >2,0 mmol/l och bör inte användas om TG är > 4,5 mmol/l. Som alternativ finns det metoder som direkt mäter LDL-kolesterol.19
Non-HDL-C och ApoB
Alternativt till LDL-C kan även non-HDL-C beräknas (non-HDL-C=TC – HDL-C). Non-HDL-C är ett mått för allt kolesterol som transporteras i ApoB-lipoproteiner (se avsnitt lipoproteiner ovan).2018
Även ApoB koncentrationen kan användas för riskbedömning och, som alternativ till LDL-C, för styrning av behandling (målvärde se tabell 3 nedan).18
I normalfallet är LDL-C, non-HDL-C och ApoB-koncentrationer höggradigt korrelerande, det vill säga är i princip utbytbara för bedömning av aterosklerotisk risk.21202223 Hos patienter med diabetes, fetma, höga triglycerid- eller mycket låga LDL-C koncentrationer kan LDL-C underskattas och ESC rekommenderar (ESC Class IC)24 användning av ApoB och/eller Non-HDL-C för riskvärdering, ApoB kan då användas som alternativ till LDL-C för screening, diagnos och terapistyrning.25
Lipoprotein(a)
ESC rekommederar att Lp(a) mäts åtminstone en gång hos varje person, för att upptäcka personer med ärftligt mycket höga Lp(a) nivåer på ≥180 mg/dl (≥430 nml/l) (ESC Class IIaC)26
Se även Lipoprotein(a) in atherosclerotic cardiovascular disease and aortic stenosis: a European Atherosclerosis Society consensus statement (EHJ 2022)27
Prover behöver inte tas fastande
Kolesterolprover som tas för screening hos patienter i primärvården eller på sjukhuset, eller som tas vid insättning av sekundärprevention för till exempel hjärtinfarktpatienter, behöver inte tas fastande. Det som skiljer sig mellan fastande och icke-fastande prover är i första hand triglycerid-koncentrationen, skillnaden ligger ofta runt 0,.3 mmol/l. Denna skillnaden spelar i de flesta fall inte någon praktisk roll. Hos patienter med metabolt syndrom, diabetes eller hypertriglyceridemi bör prover dock tas fastande.28.
När behandla hyperkolesterolemi? Intervention beroende på risk och LDL-C
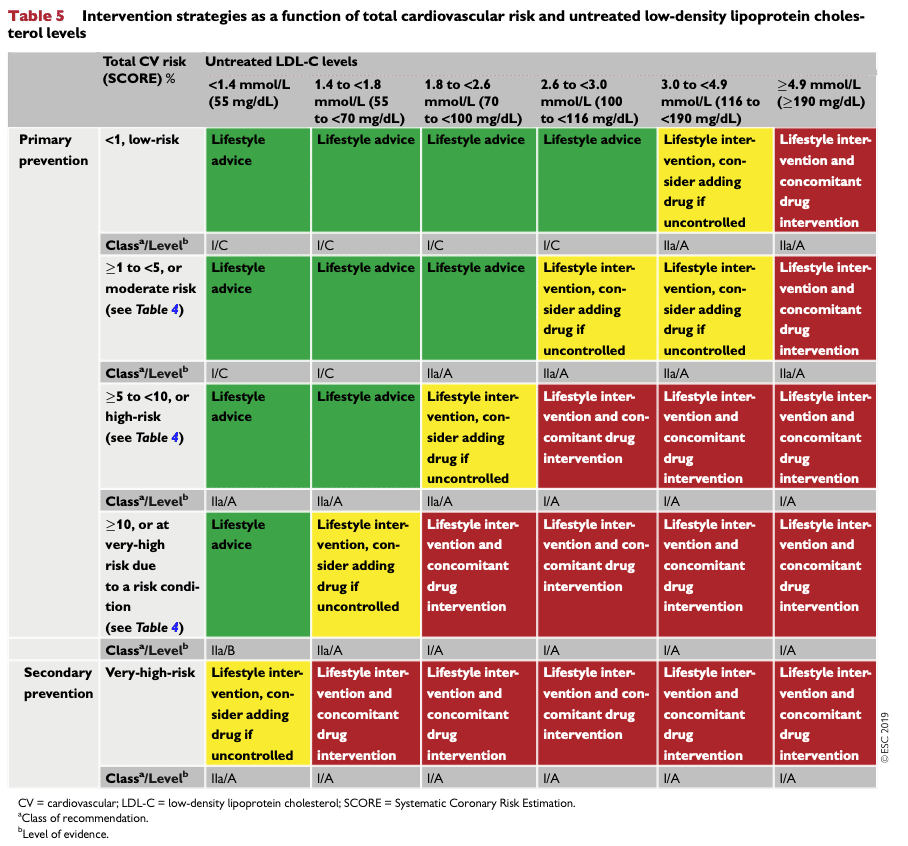
Tabellen (ESC-table 5) visar när livsstilsintervention och medikamentell kolesterolbehandling är indicerat. Målvärden visas i nästa avsnitt.
Notera att all sekundärprevention (se “riskbedömning” ovan för definition) visas i tabellens sista rad. För patienter som ska bedömas med ESCs Score (patienter utan känd aterosklerotisk sjukdom och utan diagnos som innebär en hög eller mycket hög risk, se tabell 2 ovan och sidan Score/riskkategorier för detaljer) ska även patientens ålder (se Score/risk i yngre personer och Score/risk i äldre personer) och flera riskmodifikatorer beaktas innan beslutet om insättning av läkemedelsbehandling fattas med hänsyn till helhetsbilden.
Målvärde för lipidbehandling
Tabellen nedan (blå, tabell 3) visar för varje riskgrupp målvärde för LDL-kolesterolbehandling, och alternativa målvärden för Non-HDL-C och ApoB.
| Riskkategori | Beräknad Score (Risk för kardio- vaskulär död inom 10 år) | Målvärde LDL | Målvärde Non-HDL-C | Målvärde ApoB |
|---|---|---|---|---|
| Mycket hög risk | ≥10 % | <1,4 mmol/l, + minskning minst 50% av obehandlat utgångsvärde förklaring:29 Grad av rekommendation: Sekundärprevention: ESC Class IA Primärprevention utom FH: ESC Class IC, Primärprevention vid FH: ESC Class IIaC)30 | <2,2 mmol/l | <65 mg/dl |
| Hög risk | ≥5 – 10 % | <1,8 mmol/l, + minskning minst 50% av obehandlat utgångsvärde ESC Class IA30 | <2,6 mmol/l | <80 mg/dl |
| Moderat risk | ≥1 – 5 % | <2,6 mmol/l ESC Class IIaA30 | <3,4 mmol/l | <100 mg/dl |
| Låg risk | <1 % | <3,0 mmol/l ESC Class IIbA30 |
Nästa tabell (grön, tabell 4) visar målvärde för livsstilsinterventioner (likadana för alla riskgrupper):
| Rökning | Ingen tobakprodukter oavsett typ |
| Kost | Healthy diet low in saturated fat with a focus on wholegrain products, vegetables, fruit, and fish. (se nästa avsnitt för detaljer) |
| Fysisk aktivitet | 3.5-7 h moderately vigorous physical activity per week or 30-60 min most days. |
| Vikt | BMI 20-25 kg/m2, midjemått <94 cm (män), < 80 cm (kvinnor) |
| Blodryck | <140/90 mmHg (eller lägre hos hypertonipatienter som tolererar behandlingen väl)31 |
| Triglycerider | Inget mål, men <1.7 mmol/L (<150 mg/dL) visar lägre risk |
| Diabetes | HbA1c: <7 % (<53 mmol/mol). |
Livsstilsfaktorernas roll i kolesterolbehandling
Matvanor och andra livsstilsfaktorer spelar en viktig roll i prevention av aterosklerotiska kardiovaskulära sjukdomar.
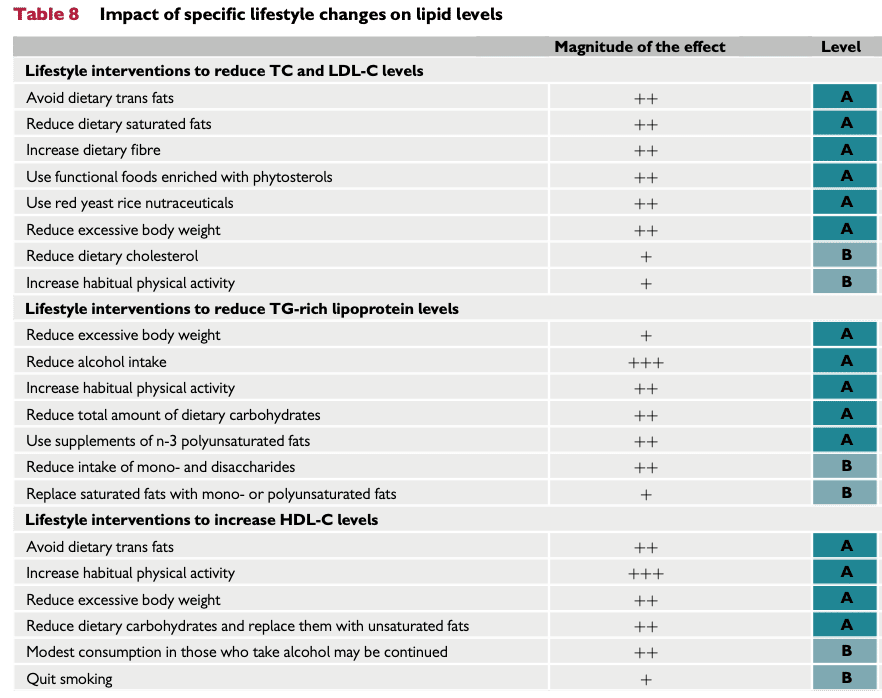
Kunskap om olika livsstilsförändringars effektstyrka på lipider sammanfattas i tabell 8 i ESC-lipidguideline 2019 :
Tabell 5: Kost-rekommendationer
| Ska föredras | Ska användas lagom | Ska endast användas ibland i begränsad mängd | |
|---|---|---|---|
| Cereals | Wholegrains | Refined bread, rice, and pasta, biscuits, corn flakes | Pastries, muffins, pies, croissants |
| Grönsaker | Råa och kokta grönsaker | Potatis | Grönsaker tillagade i smör, grädde |
| Bönor | Lentils, beans, fava beans, peas, chickpeas, soybean | ||
| Frukt | Fresh or frozen fruit | Dried fruit, jelly, jam, canned fruit, sorbets, ice lollies/popsicles, fruit juice | |
| Sötsaker | Non-caloric sweeteners | Sucrose, honey, chocolate, candy | Cookies, ice-cream, fructose, soda |
| Kött, fisk | Lean and oily fish, poultry utan skinn | Lean cuts of beef, lamb, pork, and veal, seafood, shellfish | Sausages, salami, bacon, spare ribs, hot dogs, organ meats |
| Mjölkprodukter och ägg | Skimmed milk and yoghurt | Low-fat milk, low-fat cheese and other milk products, eggs | Regular cheese, cream, whole milk and yoghurt |
| Matlagningsfett och dressing | Vinegar, mustard, fat-free dressings | Olive oil, non-tropical vegetable oils, soft margarines, salad dressing, mayonnaise, ketchup | Trans fats and hard margarines (better to avoid them), palm and coconut oils, butter, lard, bacon fat |
| Nötter/frön | All, unsalted (except coconut) | coconut | |
| Tillagning | Grilling, boiling, steaming | Stir-frying, roasting | Frying |
Läkemedelsbehandling vid hyperkolesterolemi
Innan insättning av läkemedel ska du alltid:
Innan insättning av läkemedel ska du alltid:
- Bedöma personens kardiovaskulära risk
- Patienter med sekundärpreventiv indikation: Se avsnitt ovan: bedömning av kardiovaskulär risk
- Personer där du funderar på primärpreventiv indikation: Se sidan om Score
- Slå upp individens målvärde i LDL (eller i non-HDL-C, ApoB)
- Initiera livsstilsinterventioner i patientsamtal
- Uteslut sekundära orsaker för hyperlipidemi, till exempel nefrotiskt syndrom, hypotyreos
Sedan, om läkemedelsbehandling är indicerat enligt ovan:35
- Börja behandling med en statin
- Vid sekundärprevention: Oftast lämpligt att börja direkt med högintensiv statinbehandling (Rosuvastatin 40 mg, Atorvastatin 80 mg)
- Vid primärprevention: Börja med lägre dos och titrera upp vb efter kontroll
- Läs mer om statiner (dosering, skillnader, biverkningar) på sidan statiner
- Följ upp lipidstatus efter ett par veckor:
- Är målvärdet inte nått: Öka statin till högsta tolererade dos (ESC IA) och kontrollera lipidstatus igen.36
- Om patienten inte når målvärde trots högsta tolererade dos statin: Lägg till Ezetimib 10 mg 1×1. (ESC IB)
- Tolereras statiner inte alls, inte heller efter paus + reexposition: Överväg Ezetimib 10 mg 1×1 i monoterapi (ESC IIaC)
- Följ upp lipidstatus igen:
- Om patienten inte når målvärde trots högsta tolererade dos statin + Ezetimib 10 mg 1×1:
- Sekundärprevention (mycket hög risk): Tillägg av PCSK9-hämmare rekommenderas av ESC (ESC IA)
- Primärprevention (mycket hög risk, men inte FH): Tillägg av PCSK9-hämmare kan övervägas enligt ESC (ESC IIbC)
- FH-patienter med mycket hög risk (sekundärprevention eller primärprävention + en risk faktor): (ESC IC)
- På grund av PCSK9-hämmarens höga kostnad är subventionerad användning i Sverige för nuvarande begränsad till indikationer som är mer restriktiva än ovan nämnda ESC-indikationer. En svensk beräkning kom fram till att använding av ESCs rekommendationer ovan skulle innebära att hälften av alla infarktpatienter i Sverige skulle ha en indikation för terapi med PCSK9-hämmare, vilket aktuellt inte kan anses vara ekonomiskt försvarbart.37
- TLV rekommenderar senast i 2021/02 att Repatha och Praluent subventioneras
- Sekundärprevention: LDL-C >2,5 mmol/l trots maximal tolererad statin + Ezetimib
- FH, primärprevention: LDL-C >3,0 mmol/l trots maximal tolererad statin + Ezetimib
- Se dock lokala riktlinjer i din region.
- Sekundärprevention (mycket hög risk): Tillägg av PCSK9-hämmare rekommenderas av ESC (ESC IA)
- Om patienten inte når målvärde trots högsta tolererade dos statin + Ezetimib 10 mg 1×1:
Förväntat effekt av lipidbehandling på LDL-C: 38
| Läkemedel | Förväntad LDL-C minskning |
|---|---|
| Medium-intensity statin Atorvastatin 10-20 mg Rosuvastatin 5-10 mg Pravastatin 40-80 mg Simvastatin 20-40 mg | 30 % |
| High-intensity statin Atorvastatin 40-80 mg Rosuvastatin 20-40 mg | 50 % |
| High-intensity statin + Ezetimib | 60 % |
| PCSK9-hämmare monoterapi | 60 % |
| PCSK9-hämmare + high-intensity statin | 75 % |
| PCSK9-hämmare + high-intensity statin + Ezetimib | 85 % |
Familjär Hyperkolesterolemi (FH)
Hetorozygot familjär hyperkolesterolemi är en av dem vanligaste ärftliga sjukdomar och förekommer hos cirka 1 av 250 personer. 39 Det är en autosomal dominant monogenetisk sjukdom (problemet ligger i en enda gen), i 95 % av fallen ligger mutationen i genen som kodar LDL-receptorn (>1000 mutationer är kända, varje i sig resulterande i olika grader av mindre fungerande LDL-receptorer), i övriga fall handlar det om mutationer i genen för ApoB (mutationen förändrar apoBs förmåga att koppla LDL till LDL-receptorn)40 eller PCSK9-genen (i sistnämnda fall ökar “gain of function” mutationen PCSK9-produktionen, för bakgrund se PCSK9-hämmare). Alla mutationer orskar minskat LDL-upptag i levercellen och ökade LDL-C plasmakoncentrationer. Obehandlat orsakar hetorozygot FH livslångt förhöjda kolesterolnivåer och prematur kardiovaskulär artärsjukdom. Obehandlade personer har en cirka 10 gånger högre risk för kranskärlssjukdom som ofta utvecklas innan 55 års ålder hos män och innan 60 års ålder hos kvinnor.4116
Kliniska bilden hos patienter med hetorozygot FH är kraftigt förhöjt LDL-C, och morfologiska förändringar orsakat av kroniskt höga kolesterolvärden, hos patienten själv och nära släktingar: Aterosklerotisk kärlsjukdom (ofta kranskärlssjukdom) i tidig ålder (män <55 år, kvinnor <60 år), Senxantom42 (inlagring av kolesterol i senor), Arcus cornealis43 (arcus senilis) innan 45 års ålder.
Diagnosen kan ställas kliniskt (familjehistoria, prematur kranskärslsjukdom, senxanthoma/arcus cornealis, LDL-C), med genetisk testning, eller med både och. Ett vanligt använt diagnostiskt verktyg är Dutch Lipid Clinic Network diagnoskriterier:
Dutch Lipid Clinic Network diagnoskriterier för familjär hyperkolesterolemi
- Det ska väljas max ett kriterie per grupp, är flera positiva väljs det med mer poäng.41
- >8 poäng=Definitiv FH-diagnos
- 6-8 poäng=Sannolik FH-diagnos
- 3-5 poäng= Möjlig FH-diagnos
| poäng | |
|---|---|
| Familjehistoria | |
| Förstagradssläkting med känd prematur (män <55 år; kvinnor <60 år) koronarsjukdom eller vaskulär sjukdom eller förstagradssläkting med känd LDL-C >95e percentilen | 1 |
| Förstagradssläkting med tendinous xanthomata och/eller arcus cornealis, eller barn <18 år med LDL-C >95e percentilen | 2 |
| Anamnes | |
| Patient med prematur (män <55 år; kvinnor <60 år) kranskärlssjukdom | 2 |
| Patient med prematur (män <55 år; kvinnor <60 år) cerebrovaskulär eller perifer vaskulär sjukdom | 1 |
| Status (max 6 poäng om båda kriterier finns) | |
| Senxantom42 (inlagring av kolesterol i senor) | 6 |
| Arcus cornealis43 (arcus senilis) innan 45 års ålder | 4 |
| LDL-C (värde innan behandling) | |
| LDL-C >8.5 mmol/L | 8 |
| LDL-C 6.5-8.4 mmol/L | 5 |
| LDL-C 5.0-6.4 mmol/L | 3 |
| LDL-C 4.0-4.9 mmol/L | 1 |
| DNA-analys | |
| Funktionell mutation i LDLR, apoB, eller PCSK9 gen | 8 |
Vid misstanke om FH rekommenderas remiss till en lokal lipidspecialist som bedömer indikationen för genetisk utredning och eventuell kaskadscreening av familjen, så att lipidbehandling kan påbörjas hos yngre fenotypiskt friska släktingar som ännu inte har utvecklat en aterosklerotisk kärlsjukdom.
Behandlingen av personer med diagnostiserad FH är principiellt samma som för icke-familjär hyperkolesterolemi: Först ska personens riskkategori definieras (personer med FH är antingen hög-risk eller mycket-hög risk), utifrån det ett målvärde för behandlingen definieras och sedan, om indicerat, läkemedelsbehandling inledas med statin, sedan om målet inte är nått tillägg av Ezetimib och sedan PCSK9-hämmare. Se avsnitt läkemedelsbehandling. I sällsynta fall kan LDL-aferes vara indicerat.
Homocygot FH är mycket ovanligt och förekommer med frekvens ca 1/200.000 personer, patienter har mycket höga kolesterolvärden med totalkolesterol ofta 12-30 mmol/l och utvecklar kranskärlssjukdom redan i tonåren.16
Mer info: Familial hypercholesterolaemia is underdiagnosed and undertreated in the general population: guidance for clinicians to prevent coronary heart disease: consensus statement of the European Atherosclerosis Society (EHJ 2013)16
Litteratur
2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk4
ESC guideline Lipide 2019, supplementary data
Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. A consensus statement from the European Atherosclerosis Society Consensus Panel (2017)3
Low-density lipoproteins cause atherosclerotic cardiovascular disease: pathophysiological, genetic, and therapeutic insights: a consensus statement from the European Atherosclerosis Society Consensus Panel (2020)45
Quantifying Atherogenic Lipoproteins: Current and Future Challenges in the Era of Personalized Medicine and Very Low Concentrations of LDL Cholesterol. A Consensus Statement from EAS and EFLM (2018)46
Familial hypercholesterolaemia is underdiagnosed and undertreated in the general population: guidance for clinicians to prevent coronary heart disease: consensus statement of the European Atherosclerosis Society (EHJ 2013)16
Lipoprotein(a) in atherosclerotic cardiovascular disease and aortic stenosis: a European Atherosclerosis Society consensus statement (EHJ 2022)27
Är du intresserat av forskningshistoria: A Century of Cholesterol and Coronaries: From Plaques to Genes to Statins2
Subendothelial Lipoprotein Retention as the Initiating Process in Atherosclerosis. Update and Therapeutic Implications13
Last Updated on July 3, 2024 by Christian Dworeck
- ICD-söktjänst: - August 23, 2025
- Ny sida: Var blir jag citerad? - August 13, 2025
- Ny sida: PCI vid förkalkade kranskärl – teknik, tips och evidens - May 6, 2025
- https://www.who.int [↩]
- Goldstein JL, Brown MS. A century of cholesterol and coronaries: from plaques to genes to statins. Cell. 2015 Mar 26;161(1):161-172. doi: 10.1016/j.cell.2015.01.036. PMID: 25815993; PMCID: PMC4525717. [↩] [↩] [↩] [↩]
- Ference BA, Ginsberg HN, Graham I, Ray KK, Packard CJ, Bruckert E, Hegele RA, Krauss RM, Raal FJ, Schunkert H, Watts GF, Borén J, Fazio S, Horton JD, Masana L, Nicholls SJ, Nordestgaard BG, van de Sluis B, Taskinen MR, Tokgözoglu L, Landmesser U, Laufs U, Wiklund O, Stock JK, Chapman MJ, Catapano AL. Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. A consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J. 2017 Aug 21;38(32):2459-2472. doi: 10.1093/eurheartj/ehx144. PMID: 28444290; PMCID: PMC5837225. [↩] [↩] [↩]
- Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418. [↩] [↩] [↩] [↩] [↩] [↩] [↩] [↩]
- major vascular events: hjärtinfarkt, död i kranskärlssjukdom, koronar-revaskularisering, stroke [↩]
- Cholesterol Treatment Trialists’ (CTT) Collaboration, Baigent C, Blackwell L, Emberson J, Holland LE, Reith C, Bhala N, Peto R, Barnes EH, Keech A, Simes J, Collins R. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. Lancet. 2010 Nov 13;376(9753):1670-81. doi: 10.1016/S0140-6736(10)61350-5. Epub 2010 Nov 8. PMID: 21067804; PMCID: PMC2988224. [↩]
- Ference BA, Graham I, Tokgozoglu L, Catapano AL. Impact of Lipids on Cardiovascular Health: JACC Health Promotion Series. J Am Coll Cardiol. 2018 Sep 4;72(10):1141-1156. doi: 10.1016/j.jacc.2018.06.046. PMID: 30165986. [↩]
- Baigent C, Keech A, Kearney PM, Blackwell L, Buck G, Pollicino C, Kirby A, Sourjina T, Peto R, Collins R, Simes R; Cholesterol Treatment Trialists’ (CTT) Collaborators. Efficacy and safety of cholesterol-lowering treatment: prospective meta-analysis of data from 90,056 participants in 14 randomised trials of statins. Lancet. 2005 Oct 8;366(9493):1267-78. doi: 10.1016/S0140-6736(05)67394-1. Epub 2005 Sep 27. Erratum in: Lancet. 2005 Oct 15-21;366(9494):1358. Erratum in: Lancet. 2008 Jun 21;371(9630):2084. PMID: 16214597. [↩]
- se kapitel 48 in: Md, D. Z. P., Md, L. P., Md Ms, R. B. O., Md, D. M. L., & Md, G. T. F. (2018). Braunwald’s Heart Disease: A Textbook of Cardiovascular Medicine, 2-Volume Set (11th ed.). Elsevier. [↩] [↩]
- table 6 in: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩]
- GOFMAN JW, RUBIN L, McGINLEY JP, JONES HB. Hyperlipoproteinemia. Am J Med. 1954 Oct;17(4):514-20. doi: 10.1016/0002-9343(54)90126-6. PMID: 13197415. [↩]
- Gofman JW, Delalla O, Glazier F, Freeman NK, Lindgren FT, Nichols AV, Strisower B, Tamplin AR. The serum lipoprotein transport system in health, metabolic disorders, atherosclerosis and coronary heart disease. J Clin Lipidol. 2007 May;1(2):104-41. doi: 10.1016/j.jacl.2007.03.001. PMID: 21291675. [↩]
- Tabas I, Williams KJ, Borén J. Subendothelial lipoprotein retention as the initiating process in atherosclerosis: update and therapeutic implications. Circulation. 2007 Oct 16;116(16):1832-44. doi: 10.1161/CIRCULATIONAHA.106.676890. PMID: 17938300. [↩] [↩]
- Borén J, Williams KJ. The central role of arterial retention of cholesterol-rich apolipoprotein-B-containing lipoproteins in the pathogenesis of atherosclerosis: a triumph of simplicity. Curr Opin Lipidol. 2016 Oct;27(5):473-83. doi: 10.1097/MOL.0000000000000330. PMID: 27472409. [↩]
- Tabas I, Williams KJ, Borén J. Subendothelial lipoprotein retention as the initiating process in atherosclerosis: update and therapeutic implications. Circulation. 2007 Oct 16;116(16):1832-44. doi: 10.1161/CIRCULATIONAHA.106.676890. PMID: 17938300.< [↩]
- Nordestgaard BG, Chapman MJ, Humphries SE, Ginsberg HN, Masana L, Descamps OS, Wiklund O, Hegele RA, Raal FJ, Defesche JC, Wiegman A, Santos RD, Watts GF, Parhofer KG, Hovingh GK, Kovanen PT, Boileau C, Averna M, Borén J, Bruckert E, Catapano AL, Kuivenhoven JA, Pajukanta P, Ray K, Stalenhoef AF, Stroes E, Taskinen MR, Tybjærg-Hansen A; European Atherosclerosis Society Consensus Panel. Familial hypercholesterolaemia is underdiagnosed and undertreated in the general population: guidance for clinicians to prevent coronary heart disease: consensus statement of the European Atherosclerosis Society. Eur Heart J. 2013 Dec;34(45):3478-90a. doi: 10.1093/eurheartj/eht273. Epub 2013 Aug 15. PMID: 23956253; PMCID: PMC3844152. [↩] [↩] [↩] [↩] [↩]
- Friedewald WT, Levy RI, Fredrickson DS. Estimation of the concentration of low-density lipoprotein cholesterol in plasma, without use of the preparative ultracentrifuge. Clin Chem. 1972 Jun;18(6):499-502. PMID: 4337382. [↩]
- Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩] [↩] [↩]
- Martin SS, Blaha MJ, Elshazly MB, Brinton EA, Toth PP, McEvoy JW, Joshi PH, Kulkarni KR, Mize PD, Kwiterovich PO, Defilippis AP, Blumenthal RS, Jones SR. Friedewald-estimated versus directly measured low-density lipoprotein cholesterol and treatment implications. J Am Coll Cardiol. 2013 Aug 20;62(8):732-9. doi: 10.1016/j.jacc.2013.01.079. Epub 2013 Mar 21. PMID: 23524048. [↩]
- Harari G, Green MS, Magid A, Zelber-Sagi S. Usefulness of Non-High-Density Lipoprotein Cholesterol as a Predictor of Cardiovascular Disease Mortality in Men in 22-Year Follow-Up. Am J Cardiol. 2017 Apr 15;119(8):1193-1198. doi: 10.1016/j.amjcard.2017.01.008. Epub 2017 Jan 25. PMID: 28267961. [↩] [↩]
- Emerging Risk Factors Collaboration, Di Angelantonio E, Gao P, Pennells L, Kaptoge S, Caslake M, Thompson A, Butterworth AS, Sarwar N, Wormser D, Saleheen D, Ballantyne CM, Psaty BM, Sundström J, Ridker PM, Nagel D, Gillum RF, Ford I, Ducimetiere P, Kiechl S, Koenig W, Dullaart RP, Assmann G, D’Agostino RB Sr, Dagenais GR, Cooper JA, Kromhout D, Onat A, Tipping RW, Gómez-de-la-Cámara A, Rosengren A, Sutherland SE, Gallacher J, Fowkes FG, Casiglia E, Hofman A, Salomaa V, Barrett-Connor E, Clarke R, Brunner E, Jukema JW, Simons LA, Sandhu M, Wareham NJ, Khaw KT, Kauhanen J, Salonen JT, Howard WJ, Nordestgaard BG, Wood AM, Thompson SG, Boekholdt SM, Sattar N, Packard C, Gudnason V, Danesh J. Lipid-related markers and cardiovascular disease prediction. JAMA. 2012 Jun 20;307(23):2499-506. doi: 10.1001/jama.2012.6571. PMID: 22797450; PMCID: PMC4211641. [↩]
- van den Berg MJ, van der Graaf Y, de Borst GJ, Kappelle LJ, Nathoe HM, Visseren FLJ; SMART Study Group. Low-Density Lipoprotein Cholesterol, Non-High-Density Lipoprotein Cholesterol, Triglycerides, and Apolipoprotein B and Cardiovascular Risk in Patients With Manifest Arterial Disease. Am J Cardiol. 2016 Sep 15;118(6):804-810. doi: 10.1016/j.amjcard.2016.06.048. Epub 2016 Jun 28. PMID: 27471056. [↩]
- van Deventer HE, Miller WG, Myers GL, Sakurabayashi I, Bachmann LM, Caudill SP, Dziekonski A, Edwards S, Kimberly MM, Korzun WJ, Leary ET, Nakajima K, Nakamura M, Shamburek RD, Vetrovec GW, Warnick GR, Remaley AT. Non-HDL cholesterol shows improved accuracy for cardiovascular risk score classification compared to direct or calculated LDL cholesterol in a dyslipidemic population. Clin Chem. 2011 Mar;57(3):490-501. doi: 10.1373/clinchem.2010.154773. Epub 2011 Jan 12. PMID: 21228254; PMCID: PMC4684263. [↩]
- se rekomendation p 131:Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418. [↩]
- se rek p 131 och avsnitt 5.5:Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩]
- se avsnitt 5,5 och 5.3.4 och rekommendation p 131 in: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩]
- Kronenberg F, Mora S, Stroes ESG, Ference BA, Arsenault BJ, Berglund L, Dweck MR, Koschinsky M, Lambert G, Mach F, McNeal CJ, Moriarty PM, Natarajan P, Nordestgaard BG, Parhofer KG, Virani SS, von Eckardstein A, Watts GF, Stock JK, Ray KK, Tokgözoğlu LS, Catapano AL. Lipoprotein(a) in atherosclerotic cardiovascular disease and aortic stenosis: a European Atherosclerosis Society consensus statement. Eur Heart J. 2022 Aug 29:ehac361. doi: 10.1093/eurheartj/ehac361. Epub ahead of print. PMID: 36036785. [↩] [↩]
- se avsnitt 5.4.3 in: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩]
- Med minst 50% minskning menas att <1,4
alltid ska uppnås, men målet kan bli ännu lägre än <1,4 om utgångsvärde var t.ex. 2,2, då är målet 1,1, se guideline p 132 [↩] - se tabell p 132 in: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩] [↩] [↩] [↩]
- Williams B, Mancia G, Spiering W, Agabiti Rosei E, Azizi M, Burnier M, Clement DL, Coca A, de Simone G, Dominiczak A, Kahan T, Mahfoud F, Redon J, Ruilope L, Zanchetti A, Kerins M, Kjeldsen SE, Kreutz R, Laurent S, Lip GYH, McManus R, Narkiewicz K, Ruschitzka F, Schmieder RE, Shlyakhto E, Tsioufis C, Aboyans V, Desormais I; ESC Scientific Document Group. 2018 ESC/ESH Guidelines for the management of arterial hypertension. Eur Heart J. 2018 Sep 1;39(33):3021-3104. doi: 10.1093/eurheartj/ehy339. Erratum in: Eur Heart J. 2019 Feb 1;40(5):475. PMID: 30165516. [↩]
- anpassat efter table 7 in: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418. [↩]
- table 8 in: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418. [↩]
- anpassat efter table 9 in: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418. [↩]
- avsnitt 8.1.2: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩]
- Se tabell s 145: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩]
- Allahyari A, Jernberg T, Hagström E, Leosdottir M, Lundman P, Ueda P. Application of the 2019 ESC/EAS dyslipidaemia guidelines to nationwide data of patients with a recent myocardial infarction: a simulation study. Eur Heart J. 2020 Oct 21;41(40):3900-3909. doi: 10.1093/eurheartj/ehaa034. PMID: 32072178; PMCID: PMC7654933. [↩]
- table 3, p 146 in: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩] [↩]
- Akioyamen LE, Genest J, Shan SD, Reel RL, Albaum JM, Chu A, Tu JV. Estimating the prevalence of heterozygous familial hypercholesterolaemia: a systematic review and meta-analysis. BMJ Open. 2017 Sep 1;7(9):e016461. doi: 10.1136/bmjopen-2017-016461. PMID: 28864697; PMCID: PMC5588988. [↩]
- Rader DJ, Cohen J, Hobbs HH. Monogenic hypercholesterolemia: new insights in pathogenesis and treatment. J Clin Invest. 2003 Jun;111(12):1795-803. doi: 10.1172/JCI18925. PMID: 12813012; PMCID: PMC161432. [↩]
- avsnitt 9.1: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩] [↩]
- Puttegowda B, Ali A, Ramesh B, Manjunath CN. ‘Tendon xanthomas’ as an indicator of premature coronary artery disease. Oxf Med Case Reports. 2015 Jan 24;2015(1):177-8. doi: 10.1093/omcr/omu066. PMID: 25988071; PMCID: PMC4369972. [↩] [↩]
- Barchiesi BJ, Eckel RH, Ellis PP. The cornea and disorders of lipid metabolism. Surv Ophthalmol. 1991 Jul-Aug;36(1):1-22. doi: 10.1016/0039-6257(91)90205-t. Erratum in: Surv Ophthalmol 1992 Jan-Feb;36(4):324. PMID: 1925941. [↩] [↩]
- table 12: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩]
- Borén J, Chapman MJ, Krauss RM, Packard CJ, Bentzon JF, Binder CJ, Daemen MJ, Demer LL, Hegele RA, Nicholls SJ, Nordestgaard BG, Watts GF, Bruckert E, Fazio S, Ference BA, Graham I, Horton JD, Landmesser U, Laufs U, Masana L, Pasterkamp G, Raal FJ, Ray KK, Schunkert H, Taskinen MR, van de Sluis B, Wiklund O, Tokgozoglu L, Catapano AL, Ginsberg HN. Low-density lipoproteins cause atherosclerotic cardiovascular disease: pathophysiological, genetic, and therapeutic insights: a consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J. 2020 Jun 21;41(24):2313-2330. doi: 10.1093/eurheartj/ehz962. PMID: 32052833; PMCID: PMC7308544. [↩]
- Langlois MR, Chapman MJ, Cobbaert C, Mora S, Remaley AT, Ros E, Watts GF, Borén J, Baum H, Bruckert E, Catapano A, Descamps OS, von Eckardstein A, Kamstrup PR, Kolovou G, Kronenberg F, Langsted A, Pulkki K, Rifai N, Sypniewska G, Wiklund O, Nordestgaard BG; European Atherosclerosis Society (EAS) and the European Federation of Clinical Chemistry and Laboratory Medicine (EFLM) Joint Consensus Initiative. Quantifying Atherogenic Lipoproteins: Current and Future Challenges in the Era of Personalized Medicine and Very Low Concentrations of LDL Cholesterol. A Consensus Statement from EAS and EFLM. Clin Chem. 2018 Jul;64(7):1006-1033. doi: 10.1373/clinchem.2018.287037. Epub 2018 May 14. PMID: 29760220. [↩]

