Sidoinnehåll
Bakgrund
Statiner används för att sänka plasmakoncentrationen av LDL-kolesterol och andra Apo-B-lipoproteiner hos personer med ökad kardiovaskulär risk:
Statiner minskar leverns kolesterolproduktion genom att kompetetivt hämma ett nyckelenzym i kolesterolsyntesen, HMG-CoA-reduktas. Kolesterolkoncentrationen i levercellen minskar, reaktivt ökar expressionen av LDL-receptorn på hepatocyten, och slutligen minskar koncentrationen av LDL (+ andra ApoB-lipoproteiner) i blodet.
Läs mer om bedömning av kardiovaskulär risk hos personer utan känd aterosklerotisk kardiovaskulär sjukdom på sidan om Score, och se sidan om behandlingsrekommendationer vid hyperkolesterolemi.
Statiner har effekter på LDL-kolesterol (minskning upp till ca 55 %), triglycerider (ca 10-20% reduktion) och HDL (ökning med 1-10%).1
Indikation statiner
Indikation för medikamentell lipidbehandling styrs av två faktorer: Personens kolesterolnivå och kardiovaskulära risk. Se detaljer på sidan hyperkolesterolemi (avsnitt om evidensen om statinbehandling här) och sidan om Score.
Statiner har ingen relevant effekt hos patienter med hemodialys.234
Kontraindikation
- Aktiv leversjukdom, transaminaser > 3x normalvärdet
- Samtidig behandling med glekaprevir/pibrentasvir mot hepatit C
- Överkänslighet mot läkemedlet
- Graviditet, premenopausala kvinnor som planerar graviditet eller som inte använder tillförlitlig kontraception
Se information på FASS.SE
Varning/försiktighet
Läkemedelsinteraktioner:
Alla statiner utom pravastatin metaboliseras i det hepatiska cytokrom-P systemet. Samtidig behandling med andra läkemedel som också metaboliseras via cytokrom-P kan därför öka risken för biverkningar av båda läkemedel.
- Läkemedel som metaboliseras via cytokrom P 450:5
- Anti-infektiösa:
- Itraconazol, Ketoconazol, Posaconazol
- Erythromycin, Clarithromycin
- HIV protease inhibitorer
- Calciumantagonister:
- Verapamin, Diltiazem, Amlodipin
- Andra:
- Ciclosporin, Danazol, Amiodarone, Gemfibrozil
- Grapefrukt-juice
- Anti-infektiösa:
Dosering statiner
Statiners effekt på LDL-kolesterol visar en stark interindividuell variation efter samma dos läkmedel,6 det finns alltså inte en dos som är testad i en studie och gäller för alla patienter (som t.ex vid hjärtsviktsmedicinering), rekommendationen gäller istället ett målvärde (oftast LDL, men även andra) och dosering av statin och eventuellt tillägg av andra läkemedel (i första hand Ezetimib) behöver därför justeras efter individuell lipidkontroll som alltid ska följa insätting av statiner.
Notera att olika statiner har olika genomsnittliga effektstyrkor på LDL-sänkning, t ex motsvarar 80 mg Atorvastatin ungefär 40 mg Rosuvastatin:
Statiner klassificeras efter deras effekt på LDL-kolesterol i “hight intensity”, “moderate-intensity” och low-intensity: 1
| High-intensity | Medium-intensity | Low-intensity | |
|---|---|---|---|
| LDL-reduktion | ≥ 50 % | 30-50 % | <30 % |
| Atorvastatin 40-80 mg Rosuvastatin 20-40 mg | Atorvastatin 10-20 mg Rosuvastatin 5-10 mg Pravastatin 40-80 mg Simvastatin 20-40 mg | Pravastatin 10-20 mg Simvastatin 10 mg |
För mer information om varje statins effektstyrka: Stellar trial (2003) har testat 4 olika statiner i 4 olika doseringar, respektive, på 2400 patienter med hyperkolesterolemi8. Se publikationen (table 2) för resultat.
- Atorvastatin: 10-80 mg, 1×1, morgon eller kväll
- Pravastatin: 10-80 mg, 1×1, på kvällen
- Rosuvastatin: 5-40 mg, 1×1, morgon eller kväll
- Simvastatin: 10-40 mg, 1×1, på kvällen
Innan insättning av statiner:
- Bedöm personens kardiovaskulära risk
- Patienter med sekundärpreventiv indikation: Se hyperkolesterolemi/bedömning av kardiovaskulär risk
- Personer där du funderar på primärpreventiv indikation: Se Score
- Slå upp individens målvärde i LDL (eller i non-HDL-C, ApoB)
- Initiera livsstilsinterventioner i patientsamtal
- Börja behandling med statin (och eventuellt andra läkemedel)
- Följ upp lipidstatus om ett par veckor (eventuell dosjustering eller tillägg av andra lipidsänkande läkemedel, i första hand Ezetimib)
Kontroller
- Leverprover (transaminaser, eller endast ALAT) ska tas innan behandlingsstart och 8-12 veckor efter behandlingsstart eller dosökning.9Enligt FASS.SE ska det kontrolleras “regelbundet” därefter, till exempel en gång per år. Se FASS.SE för handläggning vid transaminasstegring under behandling med statiner. Enligt ESC 201910 och FDA är dock rutinkontroller efter initierad behandling inte längre rekomenderat, eftersom allvarliga leverbiverkninar är extremt sällsynta och sannolikheten att glesa rutinkontroller skulle förhindra dessa ännu lägre.1112 Leverprover ska dock alltid tas vid klinisk misstanke om levertoxicitet (oklar svaghet, aptitlöshet, buksmärtor, ikterus, etc)13 Vid ALAT-stegring > 3x normalvärdet ska statiner sättas ut (och alternativa orsaker utredas)12
Handläggning vid ALAT-stegring: 9- ALAT < 3x övre normalvärdet: Fortsätt statinterapi oförändrat och kontrollera ALAT igen efter 4-6 veckor.
- ALAT ≥ 3x övre normalvärdet: Sätt ut eller minska statin och kontrollera igen efter 4-6 veckor.
- Om ALAT normaliseras: Försiktig återinsättning/dosökning av statin.
- OM ALAT förtsätter vara ≥ 3x normalvärdet: Fundera även på andra orsaker.
- Ta CK innan insättning av statiner (börja ej statinterapi om CK >4x normalvärdet)9 och vid vid första lipidkontrollen efter insättning av statiner och sedan vid misstanke om muskulära biverkningar (se nästa avsnitt). Det finns inga klara rekommendationer för regelbundna CK-kontroller men man kan välja att ta CK en gång per år.
Handläggning vid CK-stegring (asymptomatisk, för muskelsymptom se avsnitt biverkningar):9- CK ≥ 4 x övre normalvärdet (ULN):
- CK >10 ULN: Sätt ut statinbehandling, kontrollera njurfunktion, kontrollera CK varannan vecka.
- CK <10 ULN: Om inga symptom, fortsätt statin och kontrollera CK efter 2-6 veckor.
- CK <10 ULN: Om symptom, sätt ut statin och övervaka normalisering av CK innan reexposition med lägre dos statin.
- • Överväg om övergående CK stegring av annan orsak (ansträngning) kan föreligga.
- Fundera på myopati om CK fortsätter vara högt.
- • Överväg kombinationsterapi eller annan statin.
- CK < 4 x övre normalvärdet (ULN):
- Om inga muskulära symptom kan statinterapi fortsättas (informera patienten att höra av sig vid muskelsymptom, då ny CK kontroll).
- Om muskulära symptom: Kontrollera symptom och CK regelbundet.
- Om symptom fortsätter, sätt ut statin och re-evaluara symptomen efter 6 veckor; re-evaluara indikation för statinbehandling. •Överväg försök med återinsättning av mindre dos samma eller annan statin.
- Överväg lågdos statin, behandling varannan dag eller en/två gånger i veckan, eller kombinationsterapi.
- CK ≥ 4 x övre normalvärdet (ULN):
Biverkningar statiner
Statiner tolereas i stora majoriteten av alla fall väl. Få läkemedel är lika välstuderade som statiner. I en metaanalys som omfattade 170.000 patienter behandlade i RCT med statin vs placebo kunde ingen ökad icke-kardiovaskulär mortalitet (såsom cancer) påvisas.1415.
Muskelbiverkningar:16
- Rhabdomyolys är en allvarlig biverkning av statiner som dock är sällsynt (1-3 fall/100.000 patientår)17. Det presenterar sig med svåra muskelsmärtor och myoglobinuri som kan orsaka livshotande akut njursvikt. CK är >10x normalvärdet, ofta > 40x.
- Statin-associated muscle symptoms (SAMS) rapporteras ofta, i observationsstudier hos 10-15% av alla patienter. I randomiserade studier finns det dock ingen eller endast mycket små skillnader i SAMS mellan statin och placebo.1819 Problemet är nocebo-effekten, patientens förväntan att läkmedlet kommer att ge negativa effekter. Nocebo-effektens betydelse för SAMS testades i en elegant studie i NEJM 2020,20där patienter behandlades i intervaller med statin, placebo eller ingenting. Resultatet var att båda placebo och statin gav likadana symptom, i jämförelse med behandlingsfria intervall. Studien presenteras här:21
Läs mer om statin associerade muskelsymptom i Statin-associated muscle symptoms: impact on statin therapy-European Atherosclerosis Society Consensus Panel Statement 16
Rekomenderad handläggning vid muskulära symptom:22
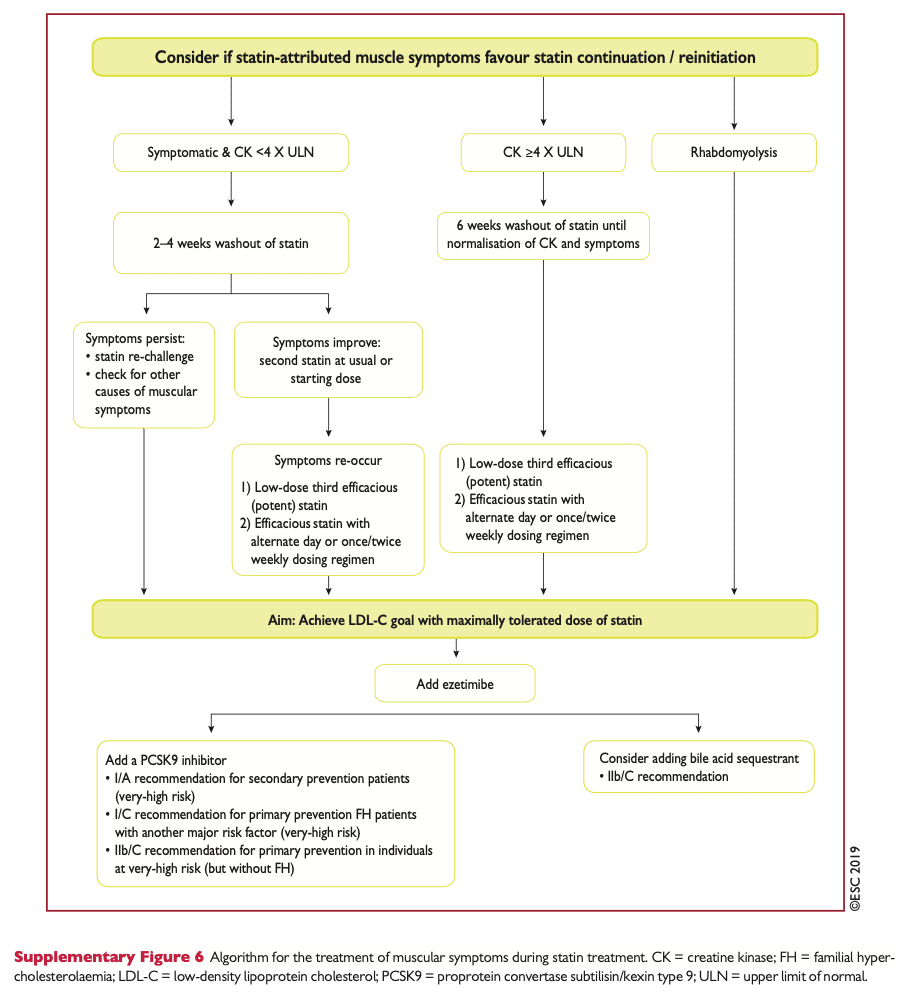
Lever-biverkningar
Mindre ökning av ALAT sker hos 0,5-2% av alla statin-behandlade patienter och kräver ingen åtgärd. ALAT-stegring till > 3 gånger normalvärdet vid 2 tidpunkter räknas som relevant23. Patienter med mindre ALAT stegringar sekundärt till steatos kan behandlas med statiner.2425 . Läs consensus-dokumentet för mer information om leverbiverkningar.26. Se även stycket om leverprover ovan i avsnitt kontroller.
Ökat risk för nydebuterad diabetes:
Statinbehandlade patienter har en ökad risk att utveckla typ 2 diabetes, en dosrelaterad effekt.26. “Number needes to cause” ett nytt fall av diabetes anges av en stor metaanlys med 255 statinbehandlade patienter; patienter med metabolt syndrom och prediabetes har högre risk än andra.27. Den stora reduktionen av kardiovaskulär risk genom statiner överväger denna mindre risk för nydebuterad diabetes.28
Relaterade sidor: Hyperkolesterolemi, Ezetimib, PCSK9-hämmare
Litteratur
2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk29
ESC guideline Lipide 2019, supplementary data
Statin-associated muscle symptoms: impact on statin therapy-European Atherosclerosis Society Consensus Panel Statement on Assessment, Aetiology and Management16
Adverse effects of statin therapy: perception vs. the evidence – focus on glucose homeostasis, cognitive, renal and hepatic function, haemorrhagic stroke and cataract. European Atherosclerosis Society Consensus Panel 2018.26
Last Updated on July 4, 2024 by Christian Dworeck
- ICD-söktjänst: - August 23, 2025
- Ny sida: Var blir jag citerad? - August 13, 2025
- Ny sida: PCI vid förkalkade kranskärl – teknik, tips och evidens - May 6, 2025
- avsnitt 8.1.2: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩] [↩]
- Cholesterol Treatment Trialists’ (CTT) Collaboration, Herrington WG, Emberson J, Mihaylova B, Blackwell L, Reith C, Solbu MD, Mark PB, Fellström B, Jardine AG, Wanner C, Holdaas H, Fulcher J, Haynes R, Landray MJ, Keech A, Simes J, Collins R, Baigent C. Impact of renal function on the effects of LDL cholesterol lowering with statin-based regimens: a meta-analysis of individual participant data from 28 randomised trials. Lancet Diabetes Endocrinol. 2016 Oct;4(10):829-39. doi: 10.1016/S2213-8587(16)30156-5. Epub 2016 Jul 29. PMID: 27477773. [↩]
- Wanner C, Krane V, März W, Olschewski M, Mann JF, Ruf G, Ritz E; German Diabetes and Dialysis Study Investigators. Atorvastatin in patients with type 2 diabetes mellitus undergoing hemodialysis. N Engl J Med. 2005 Jul 21;353(3):238-48. doi: 10.1056/NEJMoa043545. Erratum in: N Engl J Med. 2005 Oct 13;353(15):1640. PMID: 16034009. [↩]
- Fellström BC, Jardine AG, Schmieder RE, Holdaas H, Bannister K, Beutler J, Chae DW, Chevaile A, Cobbe SM, Grönhagen-Riska C, De Lima JJ, Lins R, Mayer G, McMahon AW, Parving HH, Remuzzi G, Samuelsson O, Sonkodi S, Sci D, Süleymanlar G, Tsakiris D, Tesar V, Todorov V, Wiecek A, Wüthrich RP, Gottlow M, Johnsson E, Zannad F; AURORA Study Group. Rosuvastatin and cardiovascular events in patients undergoing hemodialysis. N Engl J Med. 2009 Apr 2;360(14):1395-407. doi: 10.1056/NEJMoa0810177. Epub 2009 Mar 30. Erratum in: N Engl J Med. 2010 Apr 15;362(15):1450. PMID: 19332456. [↩]
- se table 10 i: Mach F, Ray KK, Wiklund O, Corsini A, Catapano AL, Bruckert E, De Backer G, Hegele RA, Hovingh GK, Jacobson TA, Krauss RM, Laufs U, Leiter LA, März W, Nordestgaard BG, Raal FJ, Roden M, Santos RD, Stein EA, Stroes ES, Thompson PD, Tokgözoglu L, Vladutiu GD, Gencer B, Stock JK, Ginsberg HN, Chapman MJ; European Atherosclerosis Society Consensus Panel. Adverse effects of statin therapy: perception vs. the evidence – focus on glucose homeostasis, cognitive, renal and hepatic function, haemorrhagic stroke and cataract. Eur Heart J. 2018 Jul 14;39(27):2526-2539. doi: 10.1093/eurheartj/ehy182. PMID: 29718253; PMCID: PMC6047411. [↩]
- Boekholdt SM, Hovingh GK, Mora S, Arsenault BJ, Amarenco P, Pedersen TR, LaRosa JC, Waters DD, DeMicco DA, Simes RJ, Keech AC, Colquhoun D, Hitman GA, Betteridge DJ, Clearfield MB, Downs JR, Colhoun HM, Gotto AM Jr, Ridker PM, Grundy SM, Kastelein JJ. Very low levels of atherogenic lipoproteins and the risk for cardiovascular events: a meta-analysis of statin trials. J Am Coll Cardiol. 2014 Aug 5;64(5):485-94. doi: 10.1016/j.jacc.2014.02.615. PMID: 25082583; PMCID: PMC4443441. [↩]
- se table 3: Grundy SM, Stone NJ, Bailey AL, Beam C, Birtcher KK, Blumenthal RS, Braun LT, de Ferranti S, Faiella-Tommasino J, Forman DE, Goldberg R, Heidenreich PA, Hlatky MA, Jones DW, Lloyd-Jones D, Lopez-Pajares N, Ndumele CE, Orringer CE, Peralta CA, Saseen JJ, Smith SC Jr, Sperling L, Virani SS, Yeboah J. 2018 AHA/ACC/AACVPR/AAPA/ABC/ACPM/ADA/AGS/APhA/ASPC/NLA/PCNA Guideline on the Management of Blood Cholesterol: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. J Am Coll Cardiol. 2019 Jun 25;73(24):e285-e350. doi: 10.1016/j.jacc.2018.11.003. Epub 2018 Nov 10. Erratum in: J Am Coll Cardiol. 2019 Jun 25;73(24):3237-3241. PMID: 30423393. [↩]
- Jones PH, Davidson MH, Stein EA, Bays HE, McKenney JM, Miller E, Cain VA, Blasetto JW; STELLAR Study Group. Comparison of the efficacy and safety of rosuvastatin versus atorvastatin, simvastatin, and pravastatin across doses (STELLAR* Trial). Am J Cardiol. 2003 Jul 15;92(2):152-60. doi: 10.1016/s0002-9149(03)00530-7. PMID: 12860216. [↩]
- table 13: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩] [↩] [↩] [↩]
- avsnitt 8.1.4 och table 13: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩]
- Marcum ZA, Vande Griend JP, Linnebur SA. FDA drug safety communications: a narrative review and clinical considerations for older adults. Am J Geriatr Pharmacother. 2012 Aug;10(4):264-71. doi: 10.1016/j.amjopharm.2012.05.002. Epub 2012 Jun 8. PMID: 22683398; PMCID: PMC3413741. [↩]
- se p 2537 in: Mach F, Ray KK, Wiklund O, Corsini A, Catapano AL, Bruckert E, De Backer G, Hegele RA, Hovingh GK, Jacobson TA, Krauss RM, Laufs U, Leiter LA, März W, Nordestgaard BG, Raal FJ, Roden M, Santos RD, Stein EA, Stroes ES, Thompson PD, Tokgözoglu L, Vladutiu GD, Gencer B, Stock JK, Ginsberg HN, Chapman MJ; European Atherosclerosis Society Consensus Panel. Adverse effects of statin therapy: perception vs. the evidence – focus on glucose homeostasis, cognitive, renal and hepatic function, haemorrhagic stroke and cataract. Eur Heart J. 2018 Jul 14;39(27):2526-2539. doi: 10.1093/eurheartj/ehy182. PMID: 29718253; PMCID: PMC6047411. [↩] [↩]
- se p 2537 in: Mach F, Ray KK, Wiklund O, Corsini A, Catapano AL, Bruckert E, De Backer G, Hegele RA, Hovingh GK, Jacobson TA, Krauss RM, Laufs U, Leiter LA, März W, Nordestgaard BG, Raal FJ, Roden M, Santos RD, Stein EA, Stroes ES, Thompson PD, Tokgözoglu L, Vladutiu GD, Gencer B, Stock JK, Ginsberg HN, Chapman MJ; European Atherosclerosis Society Consensus Panel. Adverse effects of statin therapy: perception vs. the evidence – focus on glucose homeostasis, cognitive, renal and hepatic function, haemorrhagic stroke and cataract. Eur Heart J. 2018 Jul 14;39(27):2526-2539. doi: 10.1093/eurheartj/ehy182. PMID: 29718253; PMCID: PMC6047411. [↩]
- Cholesterol Treatment Trialists’ (CTT) Collaboration, Baigent C, Blackwell L, Emberson J, Holland LE, Reith C, Bhala N, Peto R, Barnes EH, Keech A, Simes J, Collins R. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. Lancet. 2010 Nov 13;376(9753):1670-81. doi: 10.1016/S0140-6736(10)61350-5. Epub 2010 Nov 8. PMID: 21067804; PMCID: PMC2988224. [↩]
- Cholesterol Treatment Trialists’ (CTT) Collaboration, Emberson JR, Kearney PM, Blackwell L, Newman C, Reith C, Bhala N, Holland L, Peto R, Keech A, Collins R, Simes J, Baigent C. Lack of effect of lowering LDL cholesterol on cancer: meta-analysis of individual data from 175,000 people in 27 randomised trials of statin therapy. PLoS One. 2012;7(1):e29849. doi: 10.1371/journal.pone.0029849. Epub 2012 Jan 19. PMID: 22276132; PMCID: PMC3261846. [↩]
- Stroes ES, Thompson PD, Corsini A, Vladutiu GD, Raal FJ, Ray KK, Roden M, Stein E, Tokgözoğlu L, Nordestgaard BG, Bruckert E, De Backer G, Krauss RM, Laufs U, Santos RD, Hegele RA, Hovingh GK, Leiter LA, Mach F, März W, Newman CB, Wiklund O, Jacobson TA, Catapano AL, Chapman MJ, Ginsberg HN; European Atherosclerosis Society Consensus Panel. Statin-associated muscle symptoms: impact on statin therapy-European Atherosclerosis Society Consensus Panel Statement on Assessment, Aetiology and Management. Eur Heart J. 2015 May 1;36(17):1012-22. doi: 10.1093/eurheartj/ehv043. Epub 2015 Feb 18. PMID: 25694464; PMCID: PMC4416140. [↩] [↩] [↩]
- Law M, Rudnicka AR. Statin safety: a systematic review. Am J Cardiol. 2006 Apr 17;97(8A):52C-60C. doi: 10.1016/j.amjcard.2005.12.010. Epub 2006 Feb 3. PMID: 16581329. [↩]
- Finegold JA, Manisty CH, Goldacre B, Barron AJ, Francis DP. What proportion of symptomatic side effects in patients taking statins are genuinely caused by the drug? Systematic review of randomized placebo-controlled trials to aid individual patient choice. Eur J Prev Cardiol. 2014 Apr;21(4):464-74. doi: 10.1177/2047487314525531. Epub 2014 Mar 12. PMID: 24623264. [↩]
- Naci H, Brugts J, Ades T. Comparative tolerability and harms of individual statins: a study-level network meta-analysis of 246 955 participants from 135 randomized, controlled trials. Circ Cardiovasc Qual Outcomes. 2013 Jul;6(4):390-9. doi: 10.1161/CIRCOUTCOMES.111.000071. Epub 2013 Jul 9. PMID: 23838105. [↩]
- Wood FA, Howard JP, Finegold JA, Nowbar AN, Thompson DM, Arnold AD, Rajkumar CA, Connolly S, Cegla J, Stride C, Sever P, Norton C, Thom SAM, Shun-Shin MJ, Francis DP. N-of-1 Trial of a Statin, Placebo, or No Treatment to Assess Side Effects. N Engl J Med. 2020 Nov 26;383(22):2182-2184. doi: 10.1056/NEJMc2031173. Epub 2020 Nov 15. PMID: 33196154. [↩]
- Slomski A. “Important Conversations” Are Needed to Explain the Nocebo Effect. JAMA. 2021 Feb 3. doi: 10.1001/jama.2020.25840. Epub ahead of print. PMID: 33533926. [↩]
- ESC guideline Lipider 2019, supplementary data [↩]
- avsnitt 8.1.4: Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩]
- Chalasani N, Aljadhey H, Kesterson J, Murray MD, Hall SD. Patients with elevated liver enzymes are not at higher risk for statin hepatotoxicity. Gastroenterology. 2004 May;126(5):1287-92. doi: 10.1053/j.gastro.2004.02.015. PMID: 15131789. [↩]
- Dongiovanni P, Petta S, Mannisto V, Mancina RM, Pipitone R, Karja V, Maggioni M, Kakela P, Wiklund O, Mozzi E, Grimaudo S, Kaminska D, Rametta R, Craxi A, Fargion S, Nobili V, Romeo S, Pihlajamaki J, Valenti L. Statin use and non-alcoholic steatohepatitis in at risk individuals. J Hepatol. 2015 Sep;63(3):705-12. doi: 10.1016/j.jhep.2015.05.006. Epub 2015 May 14. PMID: 25980762. [↩]
- Mach F, Ray KK, Wiklund O, Corsini A, Catapano AL, Bruckert E, De Backer G, Hegele RA, Hovingh GK, Jacobson TA, Krauss RM, Laufs U, Leiter LA, März W, Nordestgaard BG, Raal FJ, Roden M, Santos RD, Stein EA, Stroes ES, Thompson PD, Tokgözoglu L, Vladutiu GD, Gencer B, Stock JK, Ginsberg HN, Chapman MJ; European Atherosclerosis Society Consensus Panel. Adverse effects of statin therapy: perception vs. the evidence – focus on glucose homeostasis, cognitive, renal and hepatic function, haemorrhagic stroke and cataract. Eur Heart J. 2018 Jul 14;39(27):2526-2539. doi: 10.1093/eurheartj/ehy182. PMID: 29718253; PMCID: PMC6047411. [↩] [↩] [↩]
- Sattar N, Preiss D, Murray HM, Welsh P, Buckley BM, de Craen AJ, Seshasai SR, McMurray JJ, Freeman DJ, Jukema JW, Macfarlane PW, Packard CJ, Stott DJ, Westendorp RG, Shepherd J, Davis BR, Pressel SL, Marchioli R, Marfisi RM, Maggioni AP, Tavazzi L, Tognoni G, Kjekshus J, Pedersen TR, Cook TJ, Gotto AM, Clearfield MB, Downs JR, Nakamura H, Ohashi Y, Mizuno K, Ray KK, Ford I. Statins and risk of incident diabetes: a collaborative meta-analysis of randomised statin trials. Lancet. 2010 Feb 27;375(9716):735-42. doi: 10.1016/S0140-6736(09)61965-6. Epub 2010 Feb 16. PMID: 20167359. [↩]
- Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418. [↩]
- Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, Badimon L, Chapman MJ, De Backer GG, Delgado V, Ference BA, Graham IM, Halliday A, Landmesser U, Mihaylova B, Pedersen TR, Riccardi G, Richter DJ, Sabatine MS, Taskinen MR, Tokgozoglu L, Wiklund O; ESC Scientific Document Group. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020 Jan 1;41(1):111-188. doi: 10.1093/eurheartj/ehz455. PMID: 31504418 [↩]

